文章信息
- 许玉霞,张华锋,李长岭. 2015
- XU Yuxia, ZHANG Huafeng, LI Changling. 2015
- 阿比特龙联合泼尼松治疗去势抗拒前列腺癌的临床观察
- Clinical Observation of Abriaterone Acetate and Prednison on Patients with Castrationresistant Prostate Cancer
- 肿瘤防治研究, 2015, 42(04): 382-384
- Cancer Research on Prevention and Treatment, 2015, 42(04): 382-384
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2015.04.014
-
文章历史
- 收稿日期:2014-07-31
- 修回日期:2014-10-14
2. 262599 青州,山东省青州市人民医院泌尿外科;
3.100029 北京, 中国医学科学院北京肿瘤医院
2.Department of Urology Surgery, Qingzhou People’s Hospital,Qingzhou 262599, China;
3. Beijing Cancer Hospital, Chinese Academy of Medical Science,Beijing 100029, China (*: Contributed Equally as First Author)
前列腺癌发病率在中国呈现逐年上升趋势,在老年男性60~79岁年龄段患该病概率增至13.7%,新诊断患者中位年龄为72岁。大多数前列腺癌经过中位18~24月的内分泌治疗后进展为去势抵抗性前列腺癌(castration-resistant prostate cancer,CRPC)[1, 2]。 研究表明雄激素生成及受体的活化对CRPC的进展发挥重要作用,抑制雄激素信号轴的内分泌新药可能奏效[3]。美国FDA于2011年4月28日批准新型雄激素合成抑制剂醋酸阿比特龙(Abriaterone acetate)治疗晚期CRPC患者。本研究应用醋酸阿比特龙联合泼尼松治疗去势抗拒前列腺癌患者58例,现将疗效和安全性观察结果报告如下。1 资料与方法1.1 一般资料
选取山东省青州市人民医院泌尿外科住院患者12例、中国医学科学院北京肿瘤医院泌尿外科住院患者46例,共58例去势抗拒前列腺癌患者,中位年龄68岁(61~81岁)。其中10例伴有骨转移、肝转移3例、肺转移2例、膀胱转移4例。采用欧洲泌尿外科学指南中CRPC的标准:(1)血清睾酮浓度达到去势水平(﹤1.7 nmol/L);(2)每隔两周,连续3次PSA升高,且两次PSA均较最低值升高50%;(3)抗雄激素撤退治疗无效或连续给予内分泌治疗依然出现PSA进展情况。排除患者Karnofsky体能状况评分﹤70,严重心脑血管疾病,重大手术及出血性疾病未愈者。1.2 化疗方案
醋酸阿比特龙1 g,口服;1次/日;泼尼松5 mg,2次/日,28天为一周期。化疗2周期后评价疗效及不良反应。疾病进展、严重反应或主动要求放弃治疗者终止治疗。1.3 疗效评价标准
根据实体瘤疗效评价标准(RECIST)分为完全缓解(CR)、部分缓解(PR)、疾病稳定(SD)和疾病进展(PD)。按美国NCI制定的毒性评价指标(CTC-AE3.0)对与醋酸阿比特龙治疗不良事件反应进行分级。醋酸阿比特龙治疗至少2周期后行疗效评价,每周期后记录不良反应。1.4 PSA的检测
依据美国东部肿瘤协作组提出标准,根据患者是否正常生活及患者病情,将患者健康状况视为100分,10分一个等级。采用对时间分辨荧光免疫法(TRFIA)检测前列腺特异性抗原(prostatespecific antigen,PSA)变化。化疗前后对患者Karnofsky体能状况进行评分及检测血清PSA变化。1.5 终点事件
前列腺癌相关死亡为本研究的终点事件。总生存时间(OS)为患者开始接受治疗至其死亡或末次随访时间。1.6 统计学方法
使用SPSS16.0统计软件进行数据分析,应用Kaplan-Meier法计算总生存期,在所有统计学检验中P﹤0.05为差异有统计学意义。2 结果2.1 临床疗效及生存评价
58例患者中,2例患者因严重不良反应未复查,2例患者用药未达评价时间,1例患者因经济原因停用醋酸阿比特龙。在可行评价疗效53例患者中,PR10例(18.87%),SD23例(43.40%),PD20例(37.74%),总有效率(ORR)18.87%(10例),疾病控制率(DCR)62.26%(33例);中位总生存期为(15.0±1.2)月,见图 1。
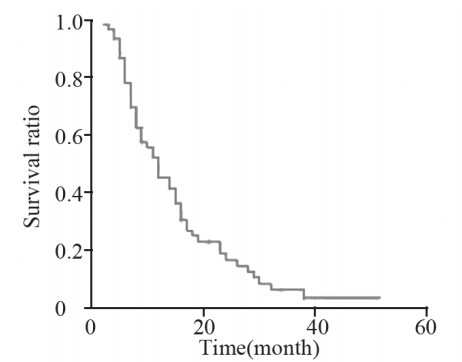 |
| 图 1 阿比特龙联合泼尼松治疗去势抗拒前列腺癌患者总生存曲线Figure 1 Overall survival curves of castration-resistant prostate cancer(CRPC) patients treated with Abriaterone acetate and prednison Figure 1 DCs infected by recombinant adenovirus (×200) |
患者治疗后Karnofsky体能状况评分增加(2.69±0.42),但与治疗前比较差异无统计学意义(P=0.319)。28例PSA下降﹥50%,治疗前后PSA中位数分别为78 ng/ml(18~1 776 ng/ml)和37 ng/ml(9~320 ng/ml),两者比较差异有统计学意义(P=0.027)。2.3 不良反应
醋酸阿比特龙总体耐受性良好,最常见的不良反应为轻度头痛、钠水潴留、低血钾、高血压、血尿、消化道反应、转氨酶升高、多为Ⅰ~Ⅱ级,心脏不良事件发生率为15%,主要表现为心动过速。骨折的发生率为6%。未发现肝功能损伤而引发肝性脑病事件发生。值得注意的是药物可能引起原有疾病加重而诱发严重心脏事件(心力衰竭),老年患者本身骨质疏松,泼尼松可能加重骨折发生。3 讨论
前列腺癌前期以手术或药物去势治疗为主,降低雄激素水平,但此后几乎所有的患者(中位缓解时间18~24月)逐渐失去对激素的敏感度,从而发展为去势抗拒的前列腺癌。有研究显示,在低水平雄激素状态下,去势抗拒前列腺癌患者雄激素受体往往被过度活化,且活化后的雄激素受体对雄激素高度敏感,这可能与雄激素受体过表达、基因扩增或点突变、受体活性构成截断拼接变异体、受体的共激活因子和共抑制因子的紊乱、激酶间信号交联所致的受体激活等相关。因此,抑制雄激素信号轴仍然是CRPC治疗的重要原因。
醋酸阿比特龙是一种新型内分泌药物,雄激素合成抑制剂。醋酸阿比特龙是靶向雄激素/受体信号通路的药物,在体内迅速转化为阿比特龙[4]。临床前研究结果显示:阿比特龙能明显抑制细胞色素氧化酶CYP17中C17裂解酶和17α羟化酶的活性,能明显抑制睾酮的前提物质(脱氢表雄酮、雄烯二酮),从而降低睾丸、前列腺和肾上腺组织中的雄激素水平,但对肾上腺的功能无影响。
一项入组21例CRPCⅠ期临床研究中,醋酸阿比特龙剂量200~2 000 mg。给药后所有患者血清睾酮和雌二醇水平均下降,部分患者的血睾丸酮在用药后8天内降至不可检测的水平[5, 6]。另一项Ⅱ期临床研究中,醋酸阿比特龙对多西他赛、酮康唑治疗失败的CRPC的PSA缓解率分别为36%、47%[7, 8]。
本研究中,在可行评价疗效53例患者中,总有效率为18.87%,疾病控制率为62.26%,结果并不满意,分析其原因,在临床实践中,患者情况复杂多样性,有因不能耐受不良反应者、经济因素等终止而行其他治疗方案,临床医师只能针对不同患者选择合适的治疗方案。对入组1 195例多西紫杉醇治疗失败的去势抗拒的前列腺癌患者Ⅲ期临床研究显示:PSA的缓解率为29.5%,客观缓解率为14.8%,总生存期分别为15.8月。本研究中,中位总生存期为(15.0±1.2)月。进一步证实了醋酸阿比特龙可以显著延长CRPC的总生存期,在临床上证实了处于去势水平的前列腺癌的进展仍然依赖于雄激素信号转导通路[9]。
本研究患者治疗后Karnofsky体能状况评分增加(2.69±0.42),但与治疗前比较差异无统计学意义(P﹥0.05),原因可能为化疗不良反应所致。阿比特龙联合泼尼松治疗33例未接受过化疗的CRPC。结果PSA缓解率67%,2例患者PSA下降至不可测量水平(0.1 ng/ml),其中11例后续随访的骨扫描示骨转移灶改善[10]。本研究28例患者PSA下降﹥50%,治疗前后PSA中位数比较差异有统计学意义(P﹤0.05),进一步说明血清PSA可作为判断疗效和检测复发的参考指标。
研究显示:对于肾功能不全、轻度肝功能不全的患者无需调整或降低剂量,而中度或重度肝功能不全的患者不宜使用阿比特龙。同时,在治疗过程中出现肝毒性的患者,应停药或适当调整剂量。本研究中钠水潴留、低血钾、高血压发生,原因可能在治疗过程中导致促肾上腺皮质激素(ACTH)和盐皮质激素分泌过多引起的,但多为Ⅰ~Ⅱ级。心脏不良事件发生率为15%,主要表现为心动过速。骨折的发生率为6%。值得注意的是药物不良引起原有疾病加重而诱发严重心脏事件(心力衰竭),骨折考虑应用泼尼松加重患者骨质疏松而导致的,醋酸阿比特龙是一个强效的去雄激素药物,同时抑制肾上腺、睾丸和前列腺雄激素的产生。理论上对初治的转移性前列腺癌以及未接受过化疗的CRPC同样具有良好的抗肿瘤作用[11, 12]。
综上所述,醋酸阿比特龙联合泼尼松对去势抗拒的前列腺癌患者的治疗是可行的,疾病控制率较高,其治疗相关的不良反应总体较轻,患者耐受性较好,但本研究的样本数较少,尚待进一步搜集大样本病例进行总结。
| [1] | Dai B, Ye DW, Kong YY, et al.Individualized prostate biopsy stategy for Chinese patients with different prostate-specific antigen levels[J]. Asian J Androc, 2008, 10(2): 325-331. |
| [2] | Ye DW, Zhu YP. Optional treatment foe hormonal refractory prostate cancer[J]. J Mod Urol, 2011, 16(1): 6-9. [叶定伟, 朱一平. 激素抵抗性前列腺癌的治疗选择[J]. 现在泌尿外科杂志, 2011, 16(1): 6-9.] |
| [3] | Nadiminty N, Gao AC. Mechanisms of persistent activation of the androgen receptor in CRPC: recent advances and future perspectives[J]. World J Urol, 2012, 30(3): 287-95. |
| [4] | Acharya M, Bernard A, Gonzalez M, et al. Open-label, phase I, pharmacokinetic studies of abiraterone acetate in healthy men[J].Cancer Chemother Pharmacol, 2012, 69(6): 1583-90. |
| [5] | Attard G, Reid AH,Yap TA, et al. Phase I clinical trial of a selective inhibitor of CYP17,abiraterone acetate,confirms that castration-resitant prostate cancer commonly remains hormone driven[J]. J Clin Oncol, 2008, 26(28): 4563-71. |
| [6] | Odonnell A, Judson I, Dowsett M, et al.Hormonal impact of the 17alpha-hydroxylase/C(17,20)-lyase inhibitor abirateron acetate(CB7630) in patients with prostate cancer[J]. Br J Cancer, 2004, 90(12): 2317-25. |
| [7] | Danila DC, Morris MJ, Debono JS, et al. Phase Ⅱ multicenter study of abiraterone acetate plus prednisone therapy in patients with docetaxed-treated castration-resistant prostate cancer[J]. J Clin Oncol, 2010, 28(9): 1496-501. |
| [8] | Ryan CJ, Smith MR, Fong L, et al. Phase I clinical trial of the CYP17 inhibitor abiraterone acetate demonstrationg clinical activity in patients with castration-resistant prosate cancer who received prior ketoconazole therapy[J].J Clin Oncol, 2010, 28(9): 1481-8. |
| [9] | de Bono JS, Logothetis CJ, Molina A, et al.Abiraterone and increased survival in metastate prostate cancer[J]. N Engl J Med, 2011, 364(21): 1995-2005. |
| [10] | Ryan CJ, ShahsS, Efstathiou E, et al. Phase Ⅱ study of abiraterone acetate in chemotherapy-na?ve metastatic castration-resistant prosate cancer displaying bone flare discordant with serologic response[J]. Clin Cancer Res, 2011, 17(14): 4854-61. |
| [11] | Ryan CJ, Li JH, Kheoh T, et al. Baseline serum adrenal androgens are prognostic and predictive of overall survival(OS) in patients with metastatic castration-resistant prosate cancer(mCRPC) : Results from the COU-AA-301 phase3 randonmized trial[C].AACR Annual Conference 103rd Annual Meeting, 2012: LB-434. |
| [12] | Ryan C, Peng W, Kheoh T, et al. Androgen dynamics and serum PSA in patients treated with abiraterone acetate[J]. Prostate Cancer Prostatic Dis, 2014, 17(2): 192-8. |
 2015, Vol. 42
2015, Vol. 42
