文章信息
- 张凯,刘培培,张伟杰,王留兴. 2014.
- ZHANG Kai, LIU Peipei, ZHANG Weijie, WANG Liuxing. 2014.
- 替吉奥胶囊联合奥沙利铂方案加贝伐单抗治疗晚期结直肠癌的临床观察
- Oxaliplatin Combined with S-1 plus Bevacizumab Regimen in Treatment of Advanced Colorectal Cancer
- 肿瘤防治研究, 2014, 41(09): 1036-1039
- Cancer Research on Prevention and Treatment, 2014, 41(09): 1036-1039
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2014.09.017
-
文章历史
- 收稿日期:2013-08-07
- 修回日期:2013-11-07
结直肠癌是常见的恶性肿瘤,约25%的结直 肠癌患者在初诊时已有潜在转移;在整个疾病进 程中,大约有50%患者出现转移[1]。因此,晚期转 移性结直肠癌的治疗是以化疗为主的综合治疗, 如何提高化疗疗效就显得愈加重要。贝伐单抗作 为血管内皮生长因子(VEGF)的人源化单克隆抗体, 通过抑制内皮细胞增殖和肿瘤新生血管生成,抗 肿瘤作用明确[2],其联合化疗具有的协同作用已 经被国外多组研究证实[3,4],因此2011年的NCCN 指南推荐贝伐单抗联合多种化疗方案作为治疗转 移性结直肠癌的标准一线化疗方案。替吉奥胶囊 联合奥沙利铂方案是治疗晚期转移性结直肠癌常 用的方案之一,但疗效还有待提高。在2013年的 ASCO会议上,The SOFT study研究[5]结果显示替 吉奥胶囊联合奥沙利铂方案加贝伐单抗治疗晚期 结直肠癌的显著疗效。本文回顾性分析分别应用 替吉奥胶囊联合奥沙利铂方案加贝伐单抗和单纯 的替吉奥胶囊联合奥沙利铂方案治疗47例晚期转 移性结直肠癌患者的临床疗效及不良反应,现报 道如下。 1 资料与方法 1.1 病例资料及分组
收集2010年6月─2012年6月郑州大学第一附 属医院肿瘤科收治的47例明确病理诊断为Ⅲ~Ⅳ期 晚期结直肠癌患者,年龄38~72岁,中位年龄56 岁,其中男20例、女27例。腺癌36例,其他类型 癌11例。所有患者Karnofsky评分均在70分以上, 治疗前血、尿常规、肝肾功能、心电图、血压、 凝血功能均在正常范围内,预计生存期在3月以 上,1月内没有接受化疗且无外伤、手术史,无中 枢神经系统转移、影像学显示无重要血管侵犯、 无不能控制的高血压;有影像学(CT/MRI)可测 量或可评价的病灶。22例患者接受替吉奥胶囊联 合奥沙利铂加贝伐单抗方案治疗,为研究组;25 例患者接受单纯替吉奥胶囊联合奥沙利铂方案化 疗,为对照组。两组临床特征差异无统计学意义 (P>0.05),见表 1。末次随访时间为2013年6月,中 位随访时间为15月。
 |
研究组治疗方案:贝伐单抗7.5 mg/kg,静脉 滴注,d1;体表面积<1.25 m2、1.25~1.50 m2、 >1.50 m2,替吉奥胶囊分别为40、50 、60毫克/次, 2次/天,连续用药2周(d1~d14);奥沙利铂130 mg/ m2, 静脉滴注,滴注时间3~6 h,d1。21天为1周期。对 照组方案:口服替吉奥胶囊剂量标准同研究组; 奥沙利铂130 mg/m2,静脉滴注,滴注时间3~6 h, d1。每治疗2周期后评价标准疗效。 1.3 疗效评定 1.3.1 近期疗效
根据实体瘤疗效评价标准 (RECIST 1.1)分为:完全缓解(CR)、部分缓 解(PR)、病变稳定(SD)、病变进展(PD); 以CR+PR为客观有效率(ORR);以CR+PR+ SD为疾病控制率(DCR);每化疗2周期后应用 CT/MRI进行对可测量病灶进行评价疗效。 1.3.2 远期疗效
无疾病进展生存期(PFS)为从 开始治疗到全身任何部位发现肿瘤进展的时间; 总生存时间(OS)为从开始治疗至患者任何原因 死亡的时间。 1.4 毒性反应
根据WHO抗癌药物急性和亚急性毒性反应分 度标准(0~Ⅳ度)评估毒性反应。 1.5 统计学方法
采用SPSS17.0软件进行分析,组间差异比较 采用χ2检验,无疾病进展生存期及中位生存期运 用Kaplan-Meier法和Log rank检验进行分析,不良 反应采用Fisher精确概率法进行检验,双侧检验以 P<0.05为差异有统计学意义。 2 结果 2.1 近期疗效
47例患者中,研究组1例、对照组3例因4~6 周期后出现疾病进展而停止用药,余患者均完成6 周期化疗,47例均可评价疗效,研究组客观有效率 (63.6%)高于对照组(36.0%),差异具有统计 学意义(χ2=4.850,P=0.028<0.05),研究组疾病控 制率(86.4%)高于对照组(68.0%),差异无统 计学意义(χ2=2.797,P=0.094>0.05),见表 2。
 |
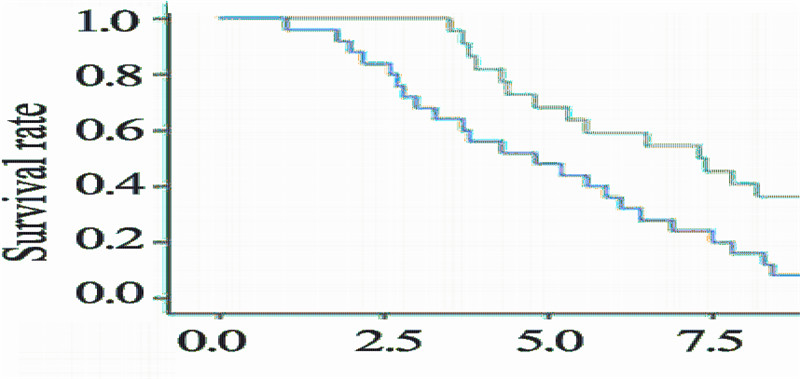
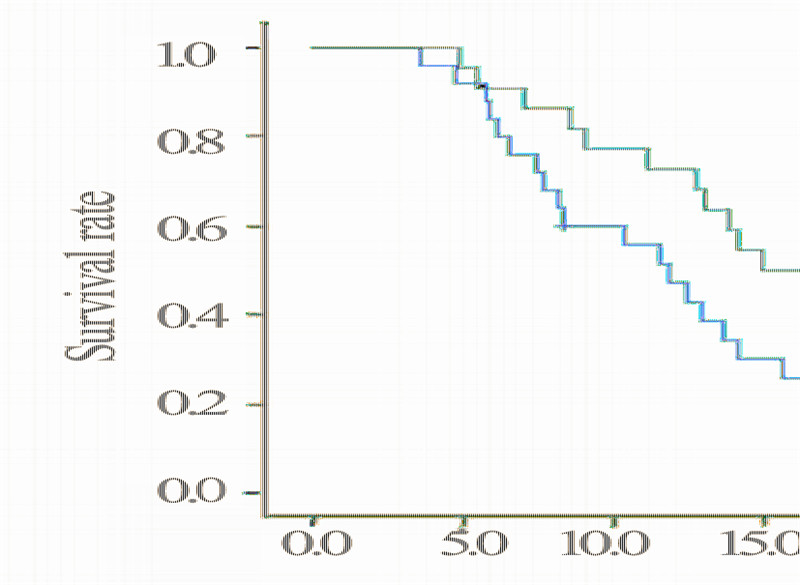
研究组的中位PFS和OS分别为7.3月(95%CI 为4.8~9.8)和15.0月(95%CI为11.2~18.8),相 对于对照组的4.8月(95%CI为2.5~7.0)和11.6月 (95%CI为5.9~17.3)均明显延长,采用Kaplan- Meier法和Log rank检验对PFS曲线和生存曲线进行 分析,χ2值分别为9.036、7.341,P<0.05,差异具 有统计学意义,见图 1、2。
|
| χ2=9.036,P=0.003 图 1 研究组与对照组晚期结直肠癌患者PFS的比较 Figure 1 PFS comparison of patients in the study group and the control group |
|
| χ2=7.341,P=0.007 图 2 研究组与对照组晚期结直肠癌患者OS的比较 Figure 2 OS comparison of patients in the study group and the control group |
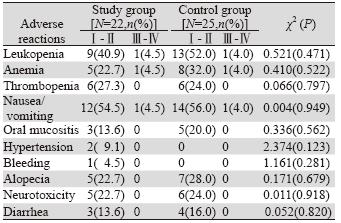
两组主要不良反应是骨髓抑制和胃肠道反 应,多为Ⅰ~Ⅱ级,给予对症处理后患者均能继续 接受化疗。实验组增加的不良反应为高血压和出 血,发生率分别为9.1%和4.5%,经药物处理均可 控制,不影响化疗连续性。两组不良反应差异无 统计学意义(P>0.05),见表 3。
 |
化疗是治疗晚期直肠癌的主要治疗手段,目前 伊立替康或奥沙利铂联合氟尿嘧啶及亚叶酸钙被认 为是治疗晚期直肠癌的标准一线治疗方案[6,7]。为 了改善氟尿嘧啶(5-Fu)持续输入所带来的不便 以及其严重的不良反应,口服5-Fu类化疗药替吉奥 胶囊问世。替吉奥胶囊是一种新型的口服氟尿嘧 啶类衍生物抗代谢类化疗药,主要由替加氟、吉 美嘧啶、奥替拉西钾组合而成。氟尿嘧啶的磷酸 化产物是氟尿嘧啶导致胃肠道不良反应的主要原 因,而奥替拉西钾的作用是能够特异性抑制肠道 黏膜细胞内乳清酸核糖转移酶阻断氟尿嘧啶的磷 酸化,因此不良反应少[8]。口服的替吉奥胶囊与持 续静脉输注的氟尿嘧啶有类似的疗效,且降低出 现血栓风险,安全性好,给药方便,患者更容易 接受,所以替吉奥胶囊联合奥沙利铂是治疗晚期 转移性结直肠癌的安全有效、方便的方案之一。
VEGF被认为是肿瘤中调节血管生成最重要的 因子,研究[9]表明高表达VEGF的肿瘤患者生存质 量明显低于VEGF 低表达或者不表达的患者,表现 在容易发生远处转移及生存率较低;其机制是与 其受体结合激活酪氨酸激酶受体,从而促进血管 内皮细胞增殖,诱导新生血管生成。贝伐单抗是 一种重组的人源化、人鼠嵌合的抗VEGF的单克隆 抗体,可通过封闭VEGF,阻断其与血管内皮细胞 生长因子受体结合,使VEGF无法活化而抑制内皮 细胞的有丝分裂,减少新生血管的形成,阻断肿 瘤生长所需的血液、氧气和其他营养供应,达到 抑制肿瘤的生长。研究表明[10]贝伐单抗还具有降 低组织间隙压,影响血管通透性,促进肿瘤血管 正常化的作用,通过增加达到肿瘤细胞的化疗药 物浓度来提高化疗疗效的目的.
Hurwitz等[11]对贝伐单抗进行的Ⅲ期临床实验 结果显示IFL联合贝伐单抗组与不联合贝伐单抗 组的ORR分别为44.9%和34.7%,OS分别为20.3月 和15.6月,PFS 分别为10.2月和6.2月,均明显高于 对照组,基于该研究结果2004 年FDA 批准其用 于转移性结直肠癌治疗。Giantonio等[12]报道贝伐 单抗联合FOLFOX方案二线治疗转移性结直肠癌 的研究结果,显示贝伐单抗组与不联合贝伐单抗 的有效率分别为21.8%和9.2%,OS分别为12.5月 和4.8月,PFS分别为7.2月和4.8月,证实了贝伐单 抗可以增加FOLFOX方案治疗晚期大肠癌的总生 存期和无进展生存期。吕强等[13]对贝伐单抗联合 CapeOx化疗用于治疗晚期转移性结直肠癌的临床 研究,结果显示:研究组ORR为74%,TTP为7.3 月;对照组ORR为42%,TTP为5.4月。本研究替 吉奥胶囊联合奥沙利铂加贝伐单抗方案治疗转移 性结直肠癌,结果表明研究组ORR和DCR分别为 63.6%、86.4%,对照组ORR和DCR分别为36.0%、 68.0%。研究组和对照组的中位PFS(7.3月vs.4.8 月)延长了2.5月,中位OS(15.0月 vs.11.6月)延长 了3.4月。本研究结果基本与吕强等报道一致; 但与国外Giantonio等[12]研究相比,PFS相一致, ORR、OS 优于其研究结果,可能原因与患者存在 个体差异有关,且本研究样本量较小,需今后扩大 样本进一步验证。
本结果中不良反应主要为恶心呕吐和骨髓抑 制,且多为Ⅰ级和Ⅱ级,Ⅲ级和Ⅳ级较少见,研 究组较对照组增加的不良反应高血压和出血的发 生率分别为9.1%、4.5%,均为Ⅰ级~Ⅱ级,经积极 对症处理后均得到缓解,且两组间差异均无统计 学意义,因此替吉奥胶囊联合奥沙利铂方案加贝 伐单抗方案治疗晚期结直肠癌疗效肯定,耐受性 较好,具有很好的临床应用前景。
| [1] | Jemal A,Siegel R,Ward E,et al.Cancer statistics,2009[J].CACancer J Clin,2009,59(4): 225-49. |
| [2] | Salgaller ML.Technology evaluation:bevacizumab,Genentech/Roche[J].Curr Opin Mol Ther,2003,5(6):657-67. |
| [3] | Chen HX, Mooney M, Boron M, et al.Phase Ⅱ multicenter trialof bevacizumab plus fluorouracil and leucovorin in patients withadvanced refractory colorectal cancer: an NCI Treatment ReferralCenter trial TRC-0301[J]. J Clin Oncol,2006,24(21):3354-60. |
| [4] | Ni TG,Guan QL,Wang N,et al.Bevacizumab plus chemotherapyas first-line therapy for metastatic colorectal cancer: asystematic review of the efficacy and safety[J].ZhongLiu,2010,30(3):232-8.[倪田根,关泉林,王娜,等. 贝伐单抗联合化疗一线治疗转移性结直肠癌有效性和安全的系统评价[J].肿瘤,2010,30(3):232-8.] |
| [5] | Daisuke T,Yasuhide Y,Hiroshi M,et al.A randomized phase Ⅲtrial of S-1/oxaliplatin (SOX) plus bevacizumab versus 5-Fu/l-LV/oxaliplatin (mFOLFOX6) plus bevacizmab in patients withmetastatic colorectal cancer: The SOFT study[J]. J Clin Oncol,2013,31(6):3519-24. |
| [6] | Giacchetti S, Perpoint B, Zidani R,et al.Phase Ⅲ multicenterrandomized trial of oxaliplatin added to chronomodulatedfluorouracil-leucovorin as first-line treatment of metastaticcolorectal cancer[J]. J Clin Oncol,2000,18(1): 136-47. |
| [7] | Douillard JY,Cunningham D,Roth AD,et al.Irinotecan combinedwith fluorouracil compared with fluorouracil alone as firstlinetreatment for metastatic colorectal cancer: a multicentrerandomised trial[J]. Lancet, 2000, 355 (9209): 1041-7. |
| [8] | Chollet P,Schoffski P,Weigang-kohler K,et al. Phase Ⅱ trial withS-1 in chemotherapy-naïve patients with gastric cancer. A trialperformed by the EORTC Early Clinical Studies Group (ECSG)[J].Eur J Cancer, 2003, 39(9): 1264-70. |
| [9] | Gerber HP, Ferrara N. The role of VEGF in normal and neoplastichematopoiesis[J]. J Mol Med, 2003,81(1): 20-31. |
| [10] | Wang Y,Fei D,Vanderlaan M,et al.Biological activity ofbevacizumab, a humanized anti-VEGF antibody in vitro[J].Angiogenesis,2004,7(4):335-45. |
| [11] | Hurwitz H, Fehrenbacher L, Novotny W, et al.Bevacizumab plusirinotecan, fluorouracil, and leucovorin for metastatic colorectalcancer[J]. N Engl J Med,2004,350(23):2335-42. |
| [12] | Giantonio BJ,Catalano PJ,Meropol NJ,et al.Bevacizumab incombination with oxaliplatin, fluorouracil, and leucovorin(FOLFOX4) for previously treated metastatic colorectal cancer:results from the Eastern Cooperative Oncology Group StudyE3200 [J]. J Clin Oncol,2007,25(12):1539-44. |
| [13] | Lv Q, Feng GG. Bevacizumab combined with CapOx in treatmentof advanced colorectal cancer[J].Xian Dai Zhong Xi Yi Jie HeZa Zhi,2011,20(18):2213-5,2218.[吕强,冯国光.贝伐单抗联合CapeOx化疗治疗晚期结直肠癌的临床研究[J].现代中西医结合杂志,2011,20(18):2213-5, 2218.] |
 2014, Vol. 41
2014, Vol. 41


