2.安徽医科大 学附属省立医院肝脏外科
2. Department of Hepatic Surgery, Affiliated Provincial Hospital of Anhui Medical University
肝细胞性肝癌是一种恶性程度高、进展快、预后 差的恶性肿瘤,占全球恶性肿瘤发病率第五位,占肿瘤 病死率第三位,占我国肿瘤病死率第二位 [1]。肝细胞性 肝癌患者大部分合并肝硬化,常伴有不同程度的门静 脉高压症及脾功能亢进[2]。肝细胞性肝癌合并门静脉 高压症有多种手术方式,如何选择最佳处理方案是肝 脏外科的重要问题[3]。阜阳市第二人民医院普外科自2006年1月—2012年10月一期联合手术治疗肝细胞性肝 癌合并门静脉高压症56例,疗效满意。现报告如下。 1 资料与方法 1.1 一般资料
本组56例患者,男38例、女18例;年龄34~61 岁,平均年龄46岁。术前肝功能Child-Pugh分级:A 级41例、B级15例。其中乙肝肝硬化49例、丙肝肝硬 化3例,不明原因肝硬化4例。患者均有不同程度的 脾肿大、脾功能亢进,其中12例有柏油便病史、7例 有呕血病史。术前均行电子胃镜检查,提示有轻度 食管胃底静脉曲张31例、中-重度曲张15例、重度食 管静脉曲张、红色征阳性10例。血小板均下降在18 ×109/L~81×109/L之间,其中PLT﹤50×109/L者 33 例, PLT﹤30×109/L者15例。1例为上消化道大出血急诊 手术,术中发现肿瘤位于左肝外侧叶,行部分肝切 除,其余为择期手术。37例行单纯脾切除术,19例 附加贲门周围血管离断术。42例行部分肝切除,其 中2例联合术中射频消融、10例行规则性左外肝切 除术、单纯术中肝癌射频消融4例。 1.2 手术方法
采用气管插管麻醉,取上腹部双侧肋缘下弧 形切口,并向剑突延伸。探查肝肿瘤部位及大 小,手术顺序多是先结扎脾动脉,分级处理脾蒂 切除脾脏,然后行贲门周围血管离断术,一般断 流至贲门上方8cm,具体断流位置要结合术前胃镜 和术中食管旁穿支血管位置高低而定。胃小弯血 管处理(分三层):先处理胃后曲张血管,然后 处理胃小弯前层腹膜结构及表层曲张血管至贲门 处,继之处理中间曲张血管及结构。对于PLT﹤30 ×109/L的15例患者,术前一天输单采血小板1个治 疗量(含血小板≥2.5×1011个),术中结扎脾动脉 或切除脾脏后再输手工采血小板1个治疗量,改善 凝血功能,最后切除肝脏肿瘤。肿瘤位于左肝外 侧叶的可以行左肝外侧叶切除术,其他部位一般 行局部肝切除,常温下间歇性阻断第一肝门或不 阻断肝门,距肿瘤边缘0.5~1.0 cm左右切除肿瘤。 对于肿瘤位置不易暴露或者肿瘤位于肝内重要血 管旁、手术切除易损伤血管的,术中在彩超引导 下行射频消融治疗。 2 结果
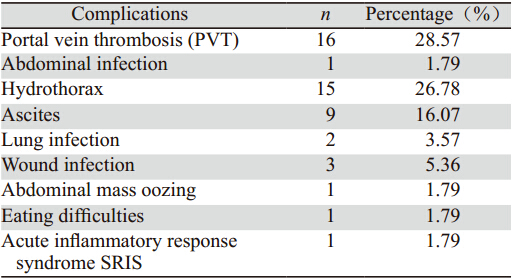
手术过程顺利,无手术死亡,手术时间2.5~5 h 之间,术中出血200~1 000 ml之间。1例术后24 h腹 腔渗血900 ml,经保守治疗后出血停止。21例术后 发热,多为门静脉血栓和反应性胸腔积液所致,积 极治疗后均好转;1例术后出现进食困难,随访1月 后缓解;1例出现急性炎症反应综合征,转ICU治 愈;腹腔感染1例、腹水9例、切口感染3例、肺部 感染2例均治愈。术后并发症见表 1。
|
|
表 1 肝细胞性肝癌合并门静脉高压症术后并发症 Table 1 Postoperative complications of hepatocellular |
本组术后随访肝功能明显改善,其中术前肝 功能Child-B级15例术后肝功能随访均达A级。1例 进食困难在胃肠功能恢复进食3天后出现,可能和 断流位置过高、进食后食物刺激等因素致食管水 肿有关,随访一月后自行缓解。随访48例患者中1 年内死亡8例,生存率83.3%,3年内死亡20例,生 存率58.3%。其中死于肝癌复发或转移18例,死于 上消化道出血1例,意外死亡1例。 3 讨论
在我国约85%~90%的肝细胞性肝癌合并有不 同程度的肝硬化,约80%合并门静脉高压症,30% 合并脾功能亢进[4]。肝细胞性肝癌合并门静脉高压 症除肝硬化因素外,还受以下因素影响:(1)肿瘤 压迫门静脉;(2)瘤内动-静脉瘘;(3)门静脉癌栓形 成阻塞血管等。由此引起门静脉高压症最主要的 病理改变是脾功能亢进和食管胃底静脉曲张,而 脾功能亢进引起的血细胞三系减少严重影响了肝 癌的多学科治疗[5]。
肝细胞性肝癌患者合并门静脉高压症患者基础 条件较差,脾肿大合并脾功能亢进,血常规提示白 细胞及血小板减少,胃镜提示食管胃底静脉曲张, 甚至部分患者既往有上消化道出血的病史,对于这 类患者往往需要解决两方面问题,其一是肝脏肿 瘤,另一是门脉高压症。是否行肝脾联合切除术, 甚至行贲门周围血管离断术,一直存在争议。如果 单纯施行肝肿瘤切除术,由于肝周较多侧支循环被 离断,术后肝脏体积减少、肝门阻断后肝脏水肿等 因素可以诱使门静脉压力进一步升高,更易发生食 管下段、胃底曲张静脉破裂出血,加之肝源性凝血 功能障碍、脾源性血小板减少、出血不易控制成为 重要致死原因[6]。若分期手术先切除脾脏和(或)贲 门周围血管,2~3月后再切除肝脏肿瘤,一方面加重 了患者的痛苦和负担,另一方面可能使肿瘤失去手 术切除的机会。有研究表明[7],肝硬化时脾脏可以抑制机体的免疫功能,即使肿瘤切除后这种抑制也 会持续存在,脾切除后消除了脾亢所致的血小板减 少,降低了门静脉压力(肝硬化门静脉高压症单纯 脾脏切除可以降低门静脉压力约30%,但联合断流 术门静脉压力变化多样),消除了食管胃底静脉曲 张的进一步加重,降低了围手术期出血的概率,减 少了术中、术后出血的风险,以及脾脏对机体免疫 功能的负面影响,脾动脉结扎可以导致肝动脉血流 相对增加,肝脏氧供增加有利于肝细胞再生和肝功 能的恢复。另外,肝癌切除术后复发多需采用TACE 等多学科治疗,脾切除后白细胞和血小板升高也为 进一步治疗创造了条件。对于有食管胃底静脉破裂 出血史或评估有出血倾向的患者要联合断流术。
肝细胞性肝癌合并脾功能亢进并不是肝癌切 除的手术禁忌证,肝切除联合脾切除往往是治疗 的选择[8, 9]。尽管肝脏联合脾脏切除和贲门周围血 管离断术增加了手术创伤,加大了手术风险,但 如果手术适应证选择恰当,联合手术是安全可行 的[8, 9, 10]。近年来局部肝切除代替了肝叶切除,提高 了肝硬化合并肝癌的手术切除率和生存率[11]。 我 们认为,一期联合手术治疗的适应证为:(1)一 般情况较好,无明显心、肺、肾等重要脏器器质 性病变;(2)肝功能正常,或仅有轻度损害,按 肝功能分级属A级;或肝功能分级B级,经短期护 肝治疗后肝功能能恢复到A级的患者;(3)无不 可切除的肝外转移性肿瘤;(4)脾功能明显亢进, 血小板<50×109/L,有出血史或胃镜下食管胃底静 脉重度曲张同时合并红色征阳性。对于肿瘤位置 不易暴露或肿瘤位于肝内重要血管旁,手术切除 易损伤血管或单个肿瘤,或癌灶在3个以内,肿瘤 直径小于3~5 cm,伴有严重的肝硬化,全肝体积 明显缩小,不能耐受肝切除者,在术中直视或超 声引导下行射频消融。本组患者中有6例患者术中 因肿瘤位置不易暴露行肝癌射频消融治疗,其中 有2例行肝癌不规则切除术的同时附加其他病灶射 频治疗,取得良好的效果。
对于食管胃底静脉曲张无红色征、无上消化道 出血的患者可单纯行脾切除,本组随访联合单纯脾 切除的仅有1例因肝癌复发门脉癌栓出现上消化道 大出血死亡。脾脏切除可以明显降低门静脉压力, 改善脾功能亢进,术中不行断流手术,也缩短了手 术时间,减低了手术对患者的创伤及术后并发症的 发生。对于有食管胃底静脉破裂出血的或胃镜下食 管、胃底静脉重度曲张同时合并红色征的患者,由 于此类患者术后上消化道出血的风险非常大,所以 需要联合贲门周围血管离断术[12],本组19例断流术 后随访的患者未出现上消化道出血。
总之,肝细胞性肝癌合并门脉高压症一期联 合手术治疗是一种安全可行的方法,联合手术同 时消除了脾亢所引起的血小板减少,降低了围手 术期的出血概率,消除了门静脉高压症出血致命 的威胁,以及脾脏对患者机体的负面影响,改善 了肝功能,也为术后综合治理提供了保障。术前 精准的评估、对适应证严格掌握,精细的术中技 术操作以及精良的管理可以最大限度减少术中及 术后并发症的发生。
| [1] | Page JM, Harrison SA. NASH and HCC[J]. Clin Liver Dis, 2009, 13(4): 631-47. |
| [2] | Wu MC, Chen H, Shen F. Surgical treatment of primary liver cancer:report of 5 524 cases[J]. Zhonghua Wai Ke Za Zhi, 2001, 39(1): 25-8.[吴孟超,陈汉,沈锋.原发性肝癌的外科治疗-附5524 例报告[J].中华外科杂志,2001,39(1):25-8.] |
| [3] | Yu LX, Li ZW,Zhang PR,et al. Surgical treatment of hepatocellular carcinoma with portal hypertension(93cases)[J]. Zhongguo Yi Yao Dao Kan,2012,14(12):2049-50.[余灵祥,李志伟,张培瑞,等.肝癌合并门静脉高压症的外科治疗(附93例报告)[J].中国医药导刊,2012,14(12):2049-50.] |
| [4] | Ganne-Carrié N,Trinchet JC.Systemic treatment of hepatocellular carcinoma[J]. Eur J Gastroenterol Hepatol,2004,16(3):275-81. |
| [5] | Shan CX,Yang N,Yang GS. Combined surgery for patiens with primary hepatocellular carcinoma complicated with severe portal hypertension[J]. Zhongguo Shi Yong Wai Ke Za Zhi, 2009, 29(5): 409-12.[单成祥,杨宁,杨广顺.同期联合手术治疗原发 性肝癌伴严重门静脉高压症疗效评价[J] .中国实用外科杂志,2009,29(5):409-12.] |
| [6] | Xu YQ, Dai CL,Bu XM,et al. Combined surgical treatment pr imar y liver cancer patients accompanied with por tal hypertension[J]. Zhongguo Yi Kan,2013,48(5):61-4.[许永庆,戴朝 六,卜献民,等.原发性肝癌合并门静脉高压症的联合手术治疗中国医刊,2013,48(5):61-4.] |
| [7] | Lao JM. Clinical research on esophageal transection portalazygos disconnection combined with liver and spleen resection in the treatment of patients with primary hepatocellular carcinoma associated with hypersplenism[J]. Zhongguo Lin Chuang Xin Yi Xue,2012,5(6):493-6.[劳景茂. 食管横断法门奇静脉断流术联合肝脾切除术治疗原发性肝癌合并脾功能亢进的临床研究[J].中国临床新医学,2012,5(6):493-6.]. |
| [8] | Sugimachi K,lkeda Y,Tomikawa M,et al. Appraisal of hepatic resection in the treatment of hepatocellular carcinoma with severe thrombocytopenia[J].World J Surg,2008,32(6):1077-81. |
| [9] | Bi XY, Zhao JJ,Yan T,et al. Peri-operative treatment for hepatocellular carcinoma patients complied with cirrhosis and hypersplenism[J].Zhonghua Wai Ke Za Zhi, 2010, 48(20): 1539-41.[毕新宇,赵建军,阎涛,等.肝癌合并肝硬化脾功能亢进的围手术期处理[J].中华外科杂志,2010,48(20):1539-41.] |
| [10] | Hirocka M,Ishida K,Kisaka Y,et al.Efficacy of splenectomy for hypersplenic patients with advanced hepatocellular carcinoma[J]. Hepatol Res,2008,38(12):1172-7. |
| [11] | Chen XP, Chen YF. The current situation and prospect in surgical treatment for hepatocellular carcinoma[J]. Lin Chuang Wai Ke Za Zhi, 2009,17(9): 579-80.[陈孝平,陈义发.肝细胞癌外科治疗现状与展望[J].临床外科杂志,2009,17(9):579-80.] |
| [12] | Jiang HC,Qiao HQ. Spleen surgery[M]. Shenyang: Liaoning Science and Technology Press, 2007:359.[姜红池,乔海泉. 脾脏外科学[M].沈阳:辽宁科学技术出版社,2007:359.] |
 2014, Vol.41
2014, Vol.41