多数类型的肿瘤,其原发灶可以得到局部控 制[1]。对原发灶一般采用局部治疗方法,例如,手 术治疗或放疗,而对转移灶的治疗一般只有系统 化疗或姑息放疗,姑息放疗一般只给予姑息剂量 以减轻症状和延缓肿瘤生长。
发生肺转移后,患者最终死于呼吸衰竭,一 般情况下只能存活一年,很少能超过2年[2]。因 此,研究能够抑制肿瘤生长而本身又对肺功能影 响不大的治疗方法都很有价值。实际上有证据表 明,手术切除肉瘤和乳腺癌的肺转移灶有可能使 患者长期生存[2],而其他微创或无创的方法也可以 用来治疗肺转移病灶。
体部立体定向放射治疗(stereotactic body radiation therapy,SBRT)能够将射野聚焦到病灶, 只给予病灶较高的剂量,而周围的正常组织只受 到较低剂量照射。国内外有多个研究将SBRT用于 治疗肺多发转移灶并取得较好的临床结果,显示 了立体定向放射治疗应用于肺多发转移灶的潜在 优势[3, 4, 5, 6]。这些研究采用的都是基于加速器的X刀 治疗,最多同时治疗4~5个病灶。体部γ刀通过多 源旋转聚焦,将剂量集中到病灶处,能够获得很 好的剂量聚焦特性,已有采用体部γ刀治疗早期非 小细胞肺癌获得95%的3年局控率的报道[7]。本研 究设计肺多发转移患者的体部γ刀计划,通过分析 剂量学数据探讨用体部γ刀治疗数目较多的肺多发 转移灶(9~12)的可行性。 1 资料和方法 1.1 病例选择
选择发生肺多发转移瘤患者20例。由于OURQGD型体部γ刀的剂量从上方锥形聚焦到焦点处, 因此根据病灶的深度采用仰卧和俯卧体位,其中 12例采用仰卧体位,8例采用俯卧体位,每个患者 一次治疗最少9个病灶,最多12个,总病灶数213 个,病灶大小0.5~2.3 cm。 1.2 OUR-QGD型体部γ刀的剂量学特点
OUR-QGD型体部γ刀的小野照射具有高斯型 的剂量分布特点,它们在空间集束聚焦照射后的 合成剂量分布具有下述特点:剂量分布集中,靶 区周边剂量变化梯度大;靶区内及靶区附近的剂 量分布不均匀,靶周边的正常组织受量小。
OUR-QGD型体部γ刀共装源30枚,钴源在源 体的分布纬度在39.5°~69.5°范围内,源体是一个 内径395 mm,外径510 mm的球冠壳体,源体旋转 时30束γ射线形成的30个锥顶角不等的射线锥面, 在焦点处聚焦,经准直体上三种孔径的圆形准直 器准直,形成10 mm、30 mm和50 mm的辐射场。 治疗过程中源体旋转形成非共面和旋转照射,具 有这两种照射方式的优点,只是非共面照射角度 比较有限。
γ刀靶点剂量场中心剂量最大,向两边缘延 伸,剂量逐渐减少。由于体部γ刀的准直孔为圆形 孔,经过准直后的每束射线都是圆锥体,30个射 束在焦点处汇交并绕Y轴旋转,形成的焦点剂量 场为椭球形,X-Z平面上是圆形,X-Y面上是椭圆 形,OUR-QGD型体部γ刀焦点剂量场X、Z轴上的 半影很小,最大不超过13 mm,Y轴半影较大,γ 刀这种剂量聚焦特性非常适合于肺多发小病灶的 治疗。 1.3 肺多发转移癌γ刀治疗计划设计 1.3.1 单靶点照射
当不规则的靶区体积缩小,形状就会趋向接 近球形。对小靶区或体积稍大而近似球形或长椭 球形(长轴在垂直方向)靶区,采用相应大小的 准直器单靶点照射,能得到处方剂量线(通常为 50%等剂量线)适形度很好的剂量分布。10 mm和 30 mm准直器单靶点照射,剂量高度聚焦,低剂量 区体积较小,特别是10 mm准直器,常用于在肺内 多发小转移灶照射,肺内体积较大的转移灶会用 到30 mm准直器单靶点照射。 1.3.2 同点混合双靶点(不同尺寸准直器)照射
采用γ刀固有的3种准直器作单靶点照射,由 于准直器尺寸的限制,无法实现对所有大小的类 球形或类椭球型靶区进行照射。需要有介于10 mm 和30 mm以及30 mm和50 mm准直器的单靶点照射 予以补充,同点混合双靶点照射可以实现这个功 能。混合双靶点和单靶点照射形成相似的剂量分 布,通常作为固有的3种准直器单靶点照射的补 充,可以看作是模拟出来的介于10 mm和30 mm及 30 mm和50 mm准直器之间的单靶点照射,还可 通过改变两个靶点的权重有限调整照射范围的大 小,用于肺转移病灶体积较大而近似球形或长椭 球形靶区照射。 1.3.3 扁椭球形(长轴在横向)靶区的照射
对于在横断面上呈扁椭球形靶区,由于单靶 点照射形成长椭球形的剂量分布,这种剂量分布 不适合扁形靶区的照射。这种情况可采用类似于 X-刀多中心照射技术,在扁椭球长轴上在适当的 距离排布靶点,调整靶点准直器大小(通常大靶 点居中,小靶点在两侧),调整靶点间的距离和 各靶点的权重以达到适形度较好的剂量分布。
PTV定义为GTV外放5 mm,下肺病灶头脚方 向PTV外放15 mm。在设计治疗计划时要求50% 等剂量线包绕PTV,同时70%等剂量线包括90% GTV。处方剂量为50%等剂量线4 Gy/f,总剂量52 Gy,换算成常规放疗剂量约为60 Gy。
对所有病例设计三维适形放疗(3DCRT)计 划,每个病灶原则上用三个射野照射,邻近的病 灶尽量用少的射野,射野方向设置尽量避免交叉 产生热点,处方剂量为70%等剂量线52 Gy包绕 PTV。将三维适形计划与γ刀计划进行比较。 1.4 统计学方法
对所有病例的每项剂量学数据求平均数和标 准差。 2 结果 2.1 γ刀给予靶区较高剂量
不论采用仰卧体位还是俯卧体位,γ刀治疗都 能很好的保护患者的肺、心脏和脊髓,见图 1~4、表 1。
处方总剂量为52 Gy时,90%的GTV靶区得到 相当于常规放疗94 Gy剂量的照射,仰卧体位双 肺的平均剂量为8.36 Gy,V20、V10和V5分别为 12.60%、24.60%和37.40%,俯卧体位双肺的平均 剂量为8.15 Gy,V20、V10和V5分别为12.67%、 25.10%和40.40%。10 Gy和20 Gy等剂量线范围比 较局限,高剂量区只集中在靶区周围,即使靶区 之间距离较近,靶区外也未出现剂量热点(剂量 大于处方剂量,且大于1.5 cm的区域)。仰卧体位 心脏所受剂量也非常低,俯卧体位即使靶区很靠 近脊髓,脊髓的剂量也比较低。
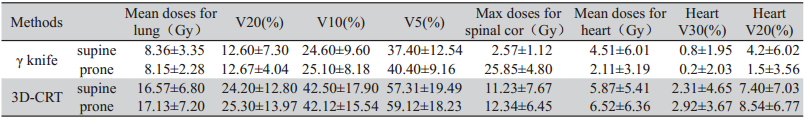
 | 图 1 仰卧病例伽玛刀和3DCRT治疗计划剂量分布比较 Figure 1 Comparison of dose distributions for a supine case between γrays radiotherapy and 3DCRT A:γrays radiotherapy;B:3 dimensional radiotherapy(3DCRT) |
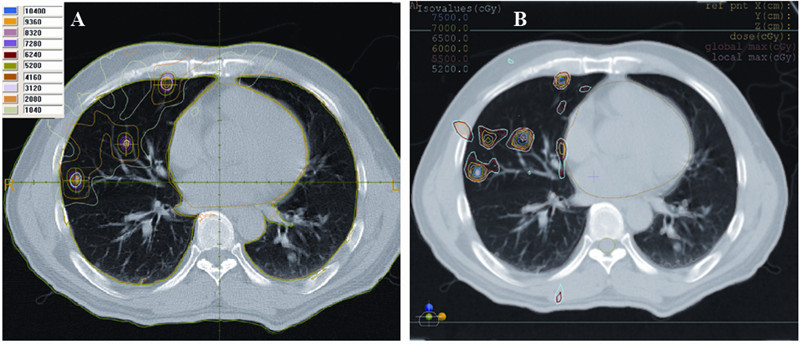
 | 图2 俯卧病例伽玛刀和3DCRT治疗计划剂量分布比较 Figure 2 Comparison of dose distributions for a prone case between γrays radiotherapy and 3DCRT A:γrays radiotherapy;B:3DCRT |
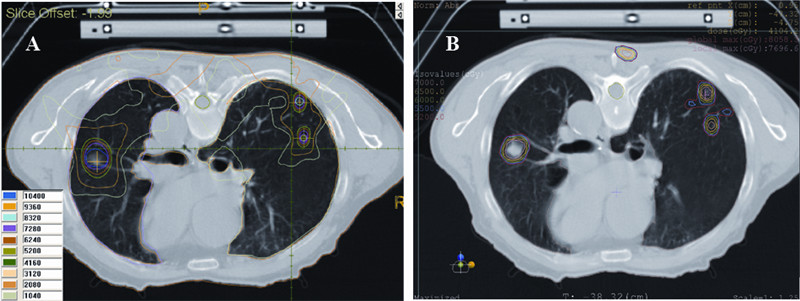
 | 图3 一个仰卧体位病例的伽玛刀DVH Figure 3 DVH of γrays radiotherapy for a supine case DVH:dose volume histogram |
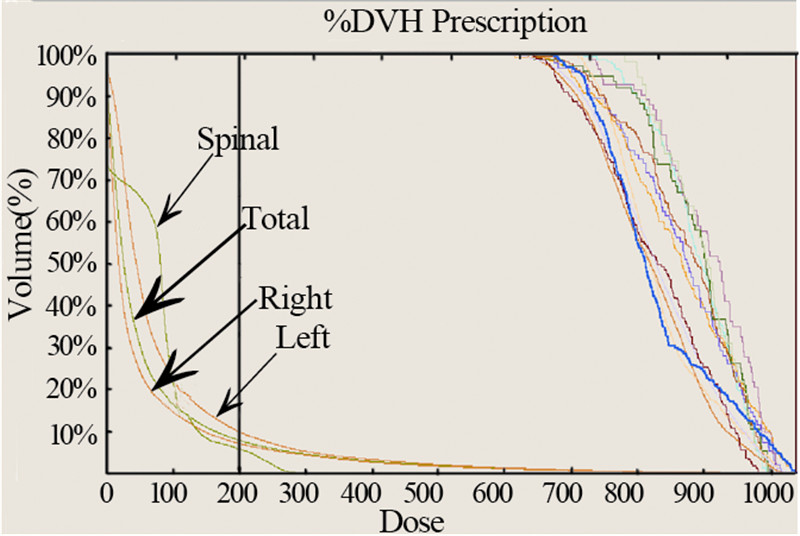 | 图4 一个俯卧体位病例的伽玛刀DVH Figure 4 DVH of γrays radiotherapy for a prone case |
|
|
表 1 伽玛刀和3DCRT治疗计划正常组织剂量 Table 1 Doses of γrays radiotherapy and 3DCRT for organs at risk |
由图 1、2可以看出,在治疗肺多发转移灶病例 中,γ刀剂量聚焦的优势在治疗相互之间距离很近 的几个小病灶中得到很好的体现。3DCRT计划中, 所有病例中最少使用了26个射野,最多使用了29 个射野。在病灶彼此比较靠近的区域,3DCRT由于 射野相互交叉,不可避免出现热点(平均有7个热 点),而γ刀的高剂量区只分布在靶区周围,避免了 靶区外热点的形成。仰卧和俯卧病例3DCRT全肺平 均剂量和V20分别为16.57 Gy、24.2%和17.13 Gy、 25.3%,均远高于γ刀的剂量学数据,见图 1、2。 3 讨论
一般认为恶性肿瘤发生肺转移,治疗应该以 全身治疗(如化疗)为主。对孤立肺转移灶, 采用局部治疗手段清除可见病灶,将有利于提 高疗效。肺转移瘤手术切除后的5年生存率可达 34%~36% [8]。放疗是肺转移瘤治疗的另一个局部 治疗手段,然而,对孤立肺转移灶采用常规放疗 技术照射,会使正常肺组织较多卷入高剂量区 内,造成不必要的放射性肺损伤,影响患者的生 活质量。
体部γ刀是采用多源线束非共面旋转聚焦的照 射方式,使高剂量区集中到肿瘤(靶区),提高肿 瘤局部的剂量,而周围正常组织的受照剂量下降迅 速,不增加正常组织的放射损伤。肺转移瘤的形态 多呈球形,膨胀性增长,因此比较适合γ刀治疗。
本文采用OUR-QGD型体部γ刀,针对肺多发 转移瘤患者设计γ刀治疗计划。结果显示γ刀能将 高剂量集中到靶区周围,即使靶区之间距离较 近,靶区外也没有出现剂量热点,在很好地保护 肺、心脏和脊髓等正常组织的同时,能够给予靶 区较高剂量。其中有些病例,由于正常组织得到 很好保护,还有提高靶区剂量和同时治疗靶区数 目的潜力,充分显示了γ刀多源旋转剂量聚焦的优 势。Okunieff等[3]采用基于加速器X刀的SBRT技术 治疗肺多发转移瘤患者,表 2是他们的剂量学数据 和本文的比较。显示采用体部γ刀单个疗程同时可 以治疗更多靶区,肺的受照剂量相当,靶区的最 小和最大剂量还有优势。
|
|
表 2 肺多发转移瘤伽玛刀治疗计划与国外SBRT计划的剂量学比较 Table 2 Dosimetic comparison of pulmonary metastases between γknife plan and SBRT plan outside China |
本文物理剂量学数据显示,采用体部γ刀治 疗数目较多的肺多发转移瘤是可行的。除了靶区 数目这个影响剂量显而易见的因素外,靶区的大 小、患者的肺体积和靶区的深度都会对剂量造成 影响。由于OUR-QGD型体部γ刀的剂量投射方式 的限制,深度较大的病灶采用俯卧体位治疗可减 少肺剂量。患者采用仰卧和俯卧两种体位同时进 行治疗,由于治疗计划系统的限制,目前还无法 对这种情况进行剂量学研究。根据目前的数据, 如果靶区数目、靶区大小合适,同时进行两种体 位的治疗也具有一定的可行性。
| [1] | Suit H,Skates S,Taghian A,et al.Clinical implications of heterogeneity of tumor response to radiation therapy[J].Radiother Oncol,1992, 25(4):251-60. |
| [2] | DeVita VT,Hellman S,Rosenberg SA.Cancer:principles and practice of oncology [M].5th ed.Philadelphia:Lippincott,1997: 252-606. |
| [3] | Okunieff P,Petersen AL,Philip A,et al.Stereotactic Body Radiation Therapy (SBRT) for lung metastases[J].Acta Oncologica,2006, 45(7): 808-17. |
| [4] | Wu SX,Deng ML,Bao Y,et al.Therapeutic analysis of stereotactic radiotherapy for 39 patients with lung metastasis[J].Ai Zheng, 2006,25(7): 880-4.[吴绍雄,邓美玲,包勇,等.39例肺转移瘤立体定向放射治疗的疗效分析[J].癌症, 2006,25(7):880-4.] |
| [5] | Xiao JP,Xu GZ,Zhang HZ,et al.Stereotactic radiotherapy for pulmonary metastatic neoplasm-preliminary experience[J]. Zhonghua Fang She Zhong Liu Xue Za Zhi,2006,15(1): 23-7.[肖建平,徐国镇,张红志,等. 肺转移瘤立体定向放疗初探[J].中华放射肿瘤学杂志,2006,15(1):23-7.] |
| [6] | Yu JM,Guo SF,Li JB,et al.Analysis of 30 cases with lung metastases treated by fractionated stereotactic radiotherapy[J].Lin Chuang Fei Ke Za Zhi,2002,7(1):21-3.[于金明,郭守芳,李建彬, 等.肺转移瘤体部X刀立体定向放射治疗30例分析[J].临床肺科杂志, 2002,7(1):21-3.] |
| [7] | Xia T,Li H,Sun Q,et al.Promising clinical outcome of stereotactic body radiation therapy for patients with inoperable stage I/II nonsmall-cell lung cancer[J].Int J Radiat Oncol Biol Phys,2006, 66(1):117-25. |
| [8] | Zheng RH,Ge D,Shi MX.Surgical treatment and prognosis of pulmonary metastasis[J].Zhonghua Jie He He Hu Xi Za Zhi,2002, 25(4): 214-7.[郑如恒, 葛棣,石美鑫.转移性肺癌的外科治疗及预后影响因素[J].中华结核和呼吸杂志,2002, 25(4): 214-7.] |
 2014, Vol.41
2014, Vol.41