特异性泛素蛋白酶22(USP22)是泛素水解酶 家族成员之一,具有去泛素的作用[1]。USP22 的N 末端是锌指结构域,能和人类染色质重塑复合体 SAGA(hSAGA )中的其他亚单位相互作用,C末端是泛素水解酶活性区,能够水解组蛋白H2A 和H2B上的泛素,从而使hSAGA 表现出转录辅助 激活因子的作用,激活靶基因转录[2]。相关研究表 明:USP22在多种实体肿瘤细胞中呈现高表达,并 且其表达程度与肿瘤转移潜能、化疗耐药性及患 者预后密切相关[3, 4, 5, 6, 7]。目前关于USP22在急性白血 病细胞中的表达情况报道较少,本研究意在探讨 USP22在急性白血病细胞中的表达及其临床意义。 1 资料与方法 1.1 研究对象
选择2012年10月—2013年6月郑州大学第一 附属医院血液内科就诊的住院患者83例为研究对 象,其中男47例,女36例,年龄16~72岁,中位年 龄为34岁。急性白血病患者诊断及缓解标准参照 张之南第三版《血液病诊断及疗效标准》[8]。另选 白血病细胞系Jurkat(急性T细胞白血病细胞)、 HL-60(人急性早幼粒白血病细胞)、K562(人 慢性髓系白血病细胞)、molt-4(人急性淋巴母细 胞性白血病细胞)和NB4(急性早幼粒细胞白血病 细胞),均由郑州大学干细胞中心提供。 1.2 研究分组
初诊组包括49例初诊为急性白血病患者,其 中急性髓系白血病(acute myeloid leukemia,AML) 31例,急性淋巴细胞性白血病(acute lymphoblastic leukemia,ALL)18例,缓解组包括19例治疗后达完 全缓解者,另选择非恶性血液系统及其他系统恶 性疾病患者15例作为阴性对照组。其中将初诊组 外周血白细胞计数≥30×109/L作为高白细胞组,将 白细胞计数<30×109/L作为非高白细胞组,初诊组 中高白细胞组32例,非高细胞组17例。 1.3 标本提取及制备
骨髓穿刺抽取骨髓液4 ml,用人外周血淋巴 细胞分离液分离出单个核细胞,分2管,分别采用 UNIQ-10柱式Trizol法提取总RNA、采用RIRA细胞 裂解液提取蛋白。另所有细胞系按照常规方法培 养于RPMI1640培养液,每3~4天传代一次,选取 处于对数生长期的细胞作为实验对象。 1.4 qRT-PCR检测USP22基因mRNA
取2 μgRNA反转录合成cDNA,进行PCR 扩增,应用SYBR® Select Master Mix 1-Pack试 剂盒(Applied Biosystem,Foster City,CA,USA) 和StepOne™Real-Time PCR System (Applied Biosystem,Foster City,CA,USA)进行此实验,根据 StepOne™Real-Time PCR(Applied Biosystem,Foster City,CA,USA)说明书进行。GAPDH基因作为内参 基因。人USP22和GAPDH 引物应用Primer Express version 2.0进行设计:USP22 mRNA引物:正义链 为5'-GGGAGGAGGCTCACCTCTAA-3',反义链 5'-AAAACCATCAACTCGGGCCT-3',产物长度113 bp;GAPDH mRNA引物:正义链为5'-TGCCCTC AACGACCACTTTG-3',反义链为5'-TCTCTCTTC CTCTTGTGCTCTTGC-3',产物长度152bp,以上 引物均由上海生工生物工程技术服务有限公司合成。
进行实时定量PCR时,USP22基因和GAPDH 在96孔板的不同孔中进行扩增,每孔的20 μl反应 体系中由Select Master Mix 1-Pack 10μl ,0.2 μM 的 正义链,0.2 μM 的反义链和25 ng的 cDNA构成, 无RNA酶余用水补足,每个样本设3个复孔。反应 参数:95℃ 10 min,95℃变性15 s,60℃退火/延 伸 1 min,共40个循环。设置溶解曲线判断是否 有非特异性的扩增和引物二聚体的出现。USP22 基因的相对表达量用2-ΔΔCt计算,ΔΔCt=(CtUSP22- CtGAPDH)实验组-(CtUSP22-CtGAPDH)对照组。 1.5 Western blot检测USP22蛋白的表达
进行聚丙烯酰胺凝胶电泳,每次两块胶。将 50 μg溶解蛋白加入5% SDS凝胶中100 V电泳30 min进行浓缩,在10% SDS凝胶中120 V电泳70 min 进行分离。将胶转移至PVDF膜(BBI,Canada), 200 mA并行转膜2 h。转膜结束后,胶和膜分别用 考马斯亮蓝和丽春红染色证明转膜成功。将膜浸 入封闭液中封闭1 h,分别加入USP22多克隆抗体 (EPITOMICS,USA) 、β-actin多克隆抗体(上海碧 云天科技有限公司)4℃孵育过夜。PBS-T洗膜三 次后,山羊抗兔二抗(BBI,Canada)25℃孵育2 h, 接下来,PBS-T洗膜三次后,根据说明书用ECL显 色法在X线片上对条带进行曝光。USP22蛋白条带 大概在60 kD处显色,β-actin蛋白大概在40 kD处显 色。对X线片进行扫描后,在电脑上通过图像处理 软件Image J进行图像分析。USP22蛋白的相对表 达量用USP22灰度值/β-actin灰度值表示。 1.6 初诊急性白血病患者的治疗情况
所有初诊急性白血病患者进行常规化疗方案 化疗,AML给予DA[柔红霉素(DNR)45~90 mg/m2 第 1~3天;阿糖胞苷(Ara-C) 100~200 mg/m2 连用7 天]或 IA[去甲氧柔红霉素(IDA)8~12 mg/m2第1~3 天;阿糖胞苷(Ara-C) 100~200 mg/m2连用7天] 方 案;ALL患者给予VDCLP[长春新碱(VCR)1.4 mg/m2,第 1、8、15、22 天;柔红霉素(DNR)40 mg/m2,第 1~3天;环磷酰胺(CTX) 750 mg/m2,第1、15天;左旋门冬酰胺酶(L-Asp) 6000 IU,第 11、14、17、20、23、26天;泼尼松 1 mg/kg连用 14天,第 15~28 天可减量1/3]方案,老年患者根 据患者情况给予剂量减量化疗,一疗程化疗后, 比较USP22表达与初诊白血病患者获得缓解情况的 关系。 1.7 统计学方法
应用统计学软件SPSS17.0分析。实验组和阴 性对照组之间的USP22基因和蛋白表达采用独立样 本t检验进行比较。显著水平用P值是否<0.05来确 定。 2 结果 2.1 实时荧光定量PCR结果
熔解曲线 USP22、GAPDH的熔解曲线峰值 单一 ,未见杂峰信号;USP22熔解温度为85℃, GAPDH熔解温度为85℃。表明PCR参数选择适 当,USP22、GAPDH反转录引物和扩增引物能够 扩增出片段,产物特异度较好,非特异产物对结 果影响较小。 2.2 急性白血病患者实时荧光定量PCR检测结果
结果显示,USP22 mRNA在Jurkat、HL-60、 K562、molt-4和NB4细胞系的表达量分别为25.61、 29.92、24.22、23.73、26.01。USP22 mRNA在初诊 组(33.90±9.58)、缓解组(1.81±0.53)白血病患 者USP22基因表达水平明显高于阴性对照组(1.05± 0.33),且差异均具有统计学意义(P<0.001);初诊 组患者的USP22基因表达水平较缓解组患者明显增 高,差异具有统计学意义(P<0.001);高白细胞组 (45.23±10.92)较非高白细胞组(26.73±6.12)的 急性白血病患者的USP22基因表达水平高,但是初 诊AML患者和初诊ALL患者之间USP22基因的表 达差异无统计学意义(P=0.531)。 2.3 Western blot检测结果
本组病例中,有些病例骨髓单个核细胞数目 不足,因此未进行本实验,最终初诊组包括28例初次诊断为急性白血病的患者(AML 17例、ALL 11例),其中高白细胞16例,非高白细胞12例; 缓解组包括15例诊断为缓解期急性白血病的患者 (AML10例、ALL 5例);阴性对照组10例进行了 本实验。
结果显示,USP22蛋白在Jurkat、HL-60、 K562、molt-4和NB4细胞系的表达量分别为 0.69、0.78、0.64、0.44、0.49。初诊组(0.58± 0.15)、缓解组(0.10±0.03)表达明显高于阴性 对照组(0.05±0.02),差异均具有统计学意义 (P <0.001);初诊组较缓解组白血病患者相比 表达明显增高(P<0.001),高白细胞组(0.69± 0.16)较非高白细胞组(0.42±0.10)的急性白血病 患者的USP22基因表达水平高。但是初诊AML患 者和初诊ALL患者之间USP22蛋白的表达差异无统 计学意义(P=0.377)。从上述结果看,实时定量 PCR的结果与Western blot分析的结果基本一致, 见图 1。
 | 图 1 Western blot检测USP22和 β-actin 蛋白的表达Figure 1USP22 and β-actin protein expressions detected by Western blot1,2: USP22 and β-actin protein expressions in initial diagnosis group;3,4: USP22 and β-actin protein expressions in remission group;5,6: USP22 and β-actin protein expressions in negative control group;7,8,9,10,11: USP22 and β-actin protein expressions in Jurkat,HL-60,K562,molt-4 and NB4 cell lines |
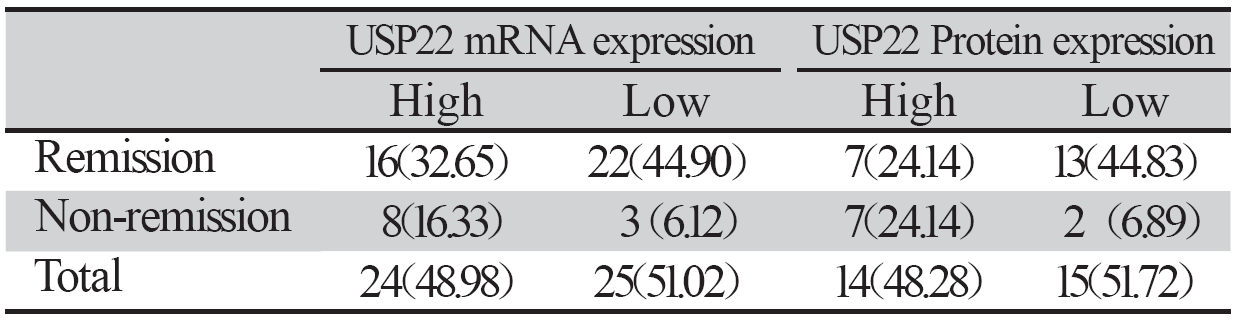
U S P 2 2 m R NA中位表达水平为3 2 . 2 2 (12.25~61.02),总初次诱导化疗缓解率为 77.55%。按照初诊USP22 mRNA中位表达水平将 初诊AL患者分为高表达组(USP22 mRNA表达> 32.22)与低表达组(USP22 mRNA表达≤32.22), 高表达组与低表达组初次诱导缓解率分别为 66.67% 、88.0%,差异有统计学意义(χ2=8.101, P=0.004),见表 1。
| 表 1 USP22 的表达与初次诱导缓解率的关系 [例(%)] Table 1 Relationship between USP22 expression and remission rate of initial diagnosis before treatment[n(%)] |
USP22蛋白中位表达水平为0.57(0.23~1.05),总初 次诱导化疗缓解率为68.96%。按照初诊USP22蛋白中位 表达水平将初诊AL患者分为高表达组(USP22蛋白表 达>0.57)与低表达组(USP22蛋白表达≤0.57),高表达 组与低表达组初次诱导缓解率分别为50%、86.67%,差 异具有统计学意义(χ2=4.392,P=0.036),见表 1。 3 讨论
USP22是泛素水解酶家族成员之一,泛素水解酶属半胱氨酸蛋白酶家族,其作用是将泛素与蛋白 底物分离开,以此来调控泛素化过程。hSAGA复合 体参与了MYC的靶基因的转录。USP22主要通过增 强C-MYC介导的基因转录,从而促进肿瘤增殖和生 长。通过RNA干扰下调USP22基因,能下调MYC介 导的靶基因转录,包括JPO1、cyclinD2、ODC、CAD 和MTA1。降低USP22表达可使高表达MYC的细胞增 殖减慢,停滞于G1期,克隆形成率下降[2],说明USP22 可以通过MYC调控的靶基因促细胞增殖、介导细胞 恶性行为[9]。相关研究证实USP22可能通过BMI-1调 控的pRb(pRb/p16INK4a/cyclin D1)[10]、p53(p14ARF/ Mdm2/P53)通路[11]和PI3k/Akt/GSK3β[12]介导细胞的恶 性增殖。此外USP22在核受体介导的基因调控、端粒 稳态维持、细胞周期调控等方面发挥着重要的生物 学功能。USP22作为一种新颖的预测转移和预后不良 的分子标记基因,已被证实在多种实体肿瘤的病理 发展过程中扮演一个重要角色,包括前列腺癌[3]、乳 腺癌[4]、肺癌[5]、胃癌[6]、大肠癌[7]等,并且其表达程度 与肿瘤转移潜能、化疗耐药性及患者预后密切相关。
本研究发现,USP22 mRNA和蛋白在初诊急性白 血病患者中有表达,且较阴性对照组表达水平高,此 结果提示USP22基因可能参与了白血病的发生、发展 的过程。高白细胞患者USP22表达量较非高白细胞患 者表达量高,而高白细胞白血病是急性白血病的高危 类型,早期死亡率高,对化疗的反应不敏感,治疗缓 解率低,总体预后不良。同时我们观察了所有初诊急 性白血病患者的情况,一疗程的标准化疗后,分析获 得完全缓解和未缓解患者的信息。与高表达USP22患 者相比,低表达USP22的患者有较高的完全缓解率, 此结果提示了高表达USP22可能是急性白血病的预 后不良的因素之一。
总之,USP22基因作为“肿瘤细胞标志物”之一, 已引起诸多肿瘤学者的重视,不仅表达与多种肿瘤疾 病,并且与急性白血病治疗的预后有关。然而USP22 如何介导白血病的生发、发展等相关机制并不明确, 尚需进一步研究。 eig
| [1] | Lee HJ, Kim MS, Shin JM, et al. The expression patterns of deubiquitinating enzymes, USP22 and Usp22[J]. Gene Expr Patterns, 2006, 6(3): 277-84. |
| [2] | Zhang XY, Varthi M, Sykes SM, et al. The putative cancer stem cell marker USP22 is a subunit of the human SAGA complex required for activated transcription and cell-cycle progression[J]. Mol Cell, 2008, 29(1): 102-11. |
| [3] | Glinsky GV. Genomic models of metastatic cancer: functional analysis of death-from-cancer signature genes reveals aneuploid, anoikis-resistant, metastasis-enabling phenotype with altered cell cycle control and activated Polycomb Group (PcG) protein chromatin silencing pathway[J]. Cell Cycle, 2006, 5(11): 1208-16. |
| [4] | Zhang Y,Yao L,Zhang X,et al. Elevated expression of USP22 in correlation with poor prognosis in patients with invasive breast cancer[J]. J Cancer Res Clin Oncol, 2011, 137(8):1245-53. |
| [5] | Hu J, Liu YL, Piao SL, et al. Expression patterns of USP22 and potential targets BMI-1, PTEN, p-AKT in non-small-cell lung cancer[J]. Lung Cancer, 2012, 77(3): 593-9. |
| [6] | Yang DD, Cui BB, Sun LY, et al. The co-expression of USP22 and BMI-1 may promote cancer progression and predict therapy failure in gastric carcinoma[J]. Cell Biochem Biophys, 2011,61(3): 703-10. |
| [7] | Zhou F,Cui BB,Liu YL,et al. Expression and clinical signifi cance of usp22 and ki67 in colorectal carcinoma[J].Zhong Liu Fang Zhi Yan Jiu ,2012,39(1):68-70.[ 周飞,崔滨滨,刘彦龙,等.USP22 和ki67在大肠癌组织中的表达及其临床意义[J].肿瘤防治研究,2012,39(1):68-70.] |
| [8] | Zhang ZN,Shen T. Haematology diagnostic and curative standard[M].Beijing:Science Press,2009: 103-34.[张之南, 沈 悌. 血液病诊断及疗效标准[M].北京:科学出版社, 2009: 103-34.] |
| [9] | Ao N,Liu YQ.Research advances in the function of USP22 in the occurrence and development of tumor[J].Ji Chu Yi Xue Yu Lin Chuang,2012, 32(10): 1235-8.[ 敖宁,刘玉琴. USP22在肿瘤发生发展中的作用研究进展[J]. 基础医学与临床, 2012,32(10): 1235-8.] |
| [10] | Liu Y,Yang Y,Xu H, et al. Implication of USP22 in the regulation of BMI-1, c-Myc, p16INK4a, p14ARF, and cyclin D2 expression in primary colorectal carcinomas[J]. Diagn Mol Pathol, 2010, 19(4): 194-200. |
| [11] | Liu YL, Jiang SX, Yang YM, et al. USP22 acts as an oncogene by the activation of BMI-1-mediated INK4a/ARF pathway and Akt pathway[J]. Cell Biochem Biophys, 2012,62(1): 229-35. |
| [12] | Song LB, Li J, Liao WT, et al. The polycomb group protein Bmi-1 represses the tumor suppressor PTEN and induces epithelialmesenchymal transition in human nasopharyngeal epithelial cells[J]. J Clin Invest, 2009,119(12): 3626-36. |
 2014, Vol.41
2014, Vol.41