文章信息
- 刘钊,张西园,马骏卿,王琳,杨玉红. 2014.
- LIU Zhao, ZHANG Xiyuan, MA Junqing, WANG Lin, YANG Yuhong. 2014.
- 小牛脾提取物注射液联合多西他赛加卡培他滨方案治疗晚期乳腺癌临床观察
- Clinical Observation of Calf Spleen Extractive Injection Combined with Docetaxel plus Capecitabine Chemotherapy in Treatment for Advanced Breast Cancer Patients
- 肿瘤防治研究, 2014, 41(10): 1116-1119
- Cancer Research on Prevention and Treatment, 2014, 41 (10): 1116-1119
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2014.10.013
-
文章历史
- 收稿日期:2013-10-08
- 修回日期:2014-06-07
乳腺癌是危害妇女健康的主要恶性肿瘤,发 病率呈上升趋势,乳腺癌患者临床确诊时5%~15% 已有远处转移,约50%患者治疗后复发转移,对此 类患者化学治疗是其主要治疗手段[1]。但许多患者 因无法耐受其不良反应而不能完成化疗方案,影 响其疗效。含蒽环类的化疗方案广泛应用于乳腺 癌的一线治疗,随着蒽环类化疗药物的耐药情况 日益增多,如何治疗蒽环类耐药的转移复发性乳 腺癌已成为临床肿瘤医生的难题。我科应用小牛 脾提取物注射液联合卡培他滨、多西他赛化疗, 用于蒽环类药物和紫杉类药物治疗失败的晚期乳 腺癌患者,观察近期疗效、免疫功能的变化及不 良反应,现报告如下。 1 资料与方法 1.1 临床资料
2006年1月至2013年1月收治对蒽环类或紫杉 类药物治疗失败的晚期乳腺癌患者106例,均为 女性,年龄30~68岁,中位年龄49岁。106例患者 均接受过含蒽环类或紫杉类药物方案化疗治疗。 所有病例原发灶均经病理学诊断为乳腺癌。其中 浸润性导管癌69例,浸润性小叶癌19例,其他类 型18例;绝经前64例,绝经后42例;雌激素受体 (ER)阳性65例,阴性41例;孕激素受体(PR) 阳性57例,阴性49例。按TNM国际标准分期,均 为Ⅲ、Ⅳ期患者、化疗前Karnofsky评分≥70分、 预计生存期>3月、近1月来未行放化疗、血常 规、肝肾功能及心电图均正常、且经组织病理学 或影像学检查确诊转移的乳腺癌患者选择入组, 均有可评价病灶。患者随机分为治疗组和对照 组,每组各53例。两组患者一般资料差异无统计 学意义(P>0.05)。 1.2 治疗方法
治疗组53例,采用多西他赛35 mg/m2,静脉滴 注,第 1、8天。卡培他滨1 000 mg/m2,每日分2次 服用,连服14天,21天为1周期。化疗同时联合应 用小牛脾提取物注射液(商品名:斯普林)20mg 加入250 ml 的0.9%氯化钠溶液或5%葡萄糖中静脉 滴注,每日1次,连用10~14天。对照组53例,单 纯应用多西他赛加卡培他滨方案化疗,21天为1周 期。化疗过程中两组治疗前1天开始常规口服地塞 米松8 mg,每日2次,连服3天,以预防多西他赛 所致的过敏反应及液体潴留,常规给予止吐、保 肝等治疗,对骨转移患者给予双膦酸盐治疗,化 疗出现骨髓抑制用粒细胞刺激因子(G-CSF)治疗。 完成2周期评估疗效,有效则继续化疗2~4周期。 1.3 疗效和毒性反应评价
治疗前后复查心电图,胸、腹部CT,每周复 查血常规、肝功能。对于治疗到达2周期或以上 者,按照WHO标准评价近期客观疗效,分为完全 缓解(CR)、部分缓解(PR)、稳定(SD)和进 展(PD),总有效率(RR)为 CR+PR 病例占可 评价疗效病例的百分数。无进展生存时间(PFS) 指从化疗开始至疾病进展或死亡。不良反应亦按 照WHO抗癌药急性与亚急性反应分级标准评定, 分为0~Ⅳ度。 1.4 临床受益反应(CBR)
CBR是评价难治性肿瘤的一个临床指标,包 括患者的疼痛强度或镇痛药用量、KPS评分和体重 是否增加3项指标。3项指标中1项有效、其他2项 稳定者为有效;3项全部稳定者为稳定;其中任何1项无效即为无效[2]。 1.5 外周血免疫指标测定
观察化疗前后T淋巴细胞亚群的变化。用流 式细胞仪检测外周血T淋巴细胞亚群(CD3+、 CD4+、CD8+、CD4+/CD8+)、自然杀伤(NK)细 胞(CD16++CD56+)占外周血淋巴细胞的比值。 1.6 统计学方法
采用SPSS16.0 统计软件包处理数据,计量资 料采用x±s表示,比较采用t检验,计数资料比较采 用χ2检验,P<0.05为差异有统计学意义。 2 结果
全组106例患者均按治疗方案顺利完成2~6周 期化疗,治疗组患者平均完成4.8周期,对照组平 均完成3.2周期,均可评价疗效及不良反应。 2.1 近期疗效
治疗组C R 1 1 例( 2 0 . 7 5 % ) ,1 8 例P R ( 3 3 . 9 6 % ) ,1 5 例SD( 2 8 . 3 0 % ) ,9 例PD (16.98%),有效率(RR)54.71%(29/53)。 对照组9例CR(16.98%),18例PR(33.96%), 14例SD(26.41%),12例PD(22.64%),有效率 (RR)为50.94%(27/53)。两组近期疗效比较, 差异无统计学意义( P>0.05) 。 2.2 无进展生存时间(PFS)
随访4~36月,中位随访时间:治疗组21.6月; 对照组11.6月。中位无进展生存时间:治疗组28.8 月,对照组6.8月。至2013年1月31日随访截止,治 疗组出现病情进展22例,死亡10例;治疗组出现 病情进展38例,死亡26例。 2.3 CBR评估
根据疼痛、KP S 评分及体质量改变3 项指 标,符合CBR标准评价的患者,治疗组4 3 例 (81.13%)有效,对照组35例有效(66.03%), 两组比较差异有统计学意义( P<0.05 )。两组对 其疼痛缓解明显,84例伴有疼痛的患者中,66 例(78.57%)止痛药物使用量减少或疼痛程度 降低≥50%。两组化疗后卡氏评分增加20分以上 的患者共 64 例(60.37%)。体质量增加者31例 (29.24%)。 2.4 不良反应
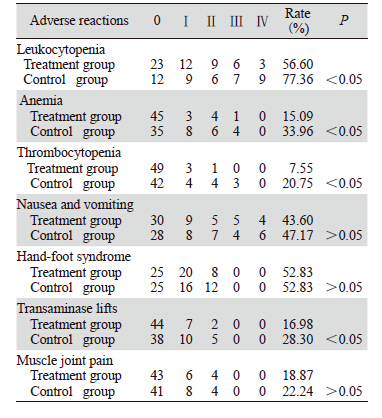
主要不良反应为骨髓抑制、手足综合征及胃 肠道反应。治疗组在外周血白细胞、血红蛋白、 血小板减少和肝功能损害方面发生率低于对照 组,差异有统计学意义(P<0.05);恶心呕吐、 手足综合征等方面,两组比较,差异无统计学意义(P>0.05),见表 1。
 |
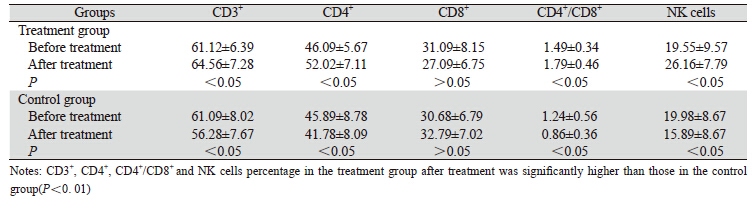
治疗后治疗组CD3+、CD4+、CD4+/CD8+、NK 细胞百分率均较治疗前及对照组升高,差异有统 计学意义(P﹤0.05;P﹤0.01)。对照组患者化 疗后CD3+、CD4+、CD4+/CD8+、NK 细胞百分率 均显著性低于化疗前,差异有统计学意义(P﹤ 0.05),见表 2。
 |
晚期乳腺癌治疗目的是尽可能缓解症状、提 高生存质量、延长生命,全身化疗是有效的治疗 手段之一。随着药物的广泛应用,越来越多患者 出现对蒽环类、紫杉醇类药物的耐药,其解救治 疗涌现出多种联合化疗方案,例如长春瑞滨、吉西他滨、多西他赛、卡培他滨等两药联合均有研 究报道[3]。一般来说在解救方案中应采用与蒽环类 药或紫杉类药无交叉耐药且有效的方案,联合治 疗优于单药。
基础研究表明乳腺癌组织中的胸腺嘧啶磷酸 化酶(TP 酶)表达阳性率高达80.9%,同时,多 西他赛可通过上调 TP 酶而与卡培他滨起协同作 用,两种药物之间一方面有明显的药理增强作 用,另一方面则作用机制不同,且无药物交叉耐 药发生,是较为理想的联合模式[4]。最近研究表 明,多西他赛联合卡培他滨治疗蒽环治疗转移性 乳腺癌失败的有效率为42%~72%[5]。理论上多西 他赛每周给药,增加药物与肿瘤细胞接触的机 会,对生长动力不同的多种靶细胞有效,与3周疗 法的标准剂量相比,剂量强度增加,血液毒性减 少。但化疗在杀灭肿瘤细胞的同时,对机体的正 常细胞亦存在杀灭作用,造成某些组织、器官功 能损害,进一步抑制其已经降低的免疫功能[6]。故 杀灭肿瘤细胞必须同时保护机体的骨髓造血功能 及机体的免疫功能。
小牛脾提取物注射液是从健康胎牛脾脏中提 取的高活性低分子活性肽,通过抑制肿瘤细胞糖 元聚集和分解过程,使能量代谢发生障碍,并使 细胞停滞G0/G1期,阻碍细胞向S期转化诱导肿瘤细 胞凋亡,抑制肿瘤细胞增殖。同时小牛脾提取物 刺激机体免疫系统,促进淋巴母细胞生成,增加 淋巴细胞数量,增强T淋巴细胞活性,提高机体免 疫力,刺激骨髓干细胞的增殖,具有升高白细胞 及血小板的作用[7]。
本研究采用小牛脾提取物注射液联合多西 他赛加卡培他滨化疗方案治疗晚期乳腺癌, 在总有效率方面,治疗组( 5 4 . 7 1 % ) 与对照 组(50.94%)相当,差异无统计学意义(P> 0.05)。中位随访时间:治疗组21.6月,对照组 11.6月;中位无进展生存时间:治疗组8.8月,对照组6.8月。但是临床受益反应评价,治疗组 (81.13%)明显高于对照组(66.03%),差异有 统计学意义(P﹤0.05)。在不良反应方面,治疗 组在外周血白细胞、血红蛋白、血小板减少和肝 功能损害方面发生率低于对照组,差异有统计学 意义(P<0.05),说明小牛脾提取物注射液具有 保护肝功能、保护骨髓、促进造血的作用。治疗 组CD3+、CD4+、CD4+ /CD8+、NK 细胞百分率均 较治疗前及对照组升高,差异有统计学意义(P﹤ 0.05;P﹤0.01)。这表明小牛脾提取物注射液能 改善晚期乳腺癌患者的T淋巴细胞NK细胞的免疫 活性。
总之,小牛脾提取物注射液联合多西他赛加 卡培他滨化疗方案治疗晚期乳腺癌,可以提高患 者对化疗的耐受性,减轻化疗后骨髓抑制,提高 抗肿瘤免疫活性,改善生活质量,延长患者生存 期。但此研究例数较少有待于多中心、大样本的 临床观察。
| [1] | Wang HQ,Qian ZZ,Liu XM,et al. Capecitabine combined with weekly docetaxel in Chinese patients >65 years with anthracycline-resistant metastatic breast cancer[J]. Chin Med J (Engl), 2010, 123(22): 3212-6. |
| [2] | Burris HA 3rd, Moore MJ,Andersen J, et al. Improvements in survival and clinical bencfit with gemcitabine as first-line therapy for patients with advanced pancreas cancer: a randomized trial[J]. J Clin Oncol, 1997, 15(6): 2403-13. |
| [3] | Schmidinger M,Budinsky AC,Wenzel C,et al.Docetaxel monotherapy in heavily pretreated metastatic breast cancer: a multicenter, community-based feasibility trial[J].Cancer Chemother Pharmacol, 2001, 47(1): 57-62. |
| [4] | Pronk LC, Vasey P, Sparreboom A, et al. A phaseⅠand pharmacokinetic study of the combination of capecitabine and docetaxel in patients with advanced solid tumours[J]. Br J Cancer, 2000, 83(1): 22-9. |
| [5] | Zhang SH, Jiang ZF, Song ST, et al. The clinical study of docetaxel-capecitabine combination in treatment of metastatic breast cancer patients failed prior treatment with anthracyclin[J]. Ai Zheng Jin Zhan, 2004, 2(3): 217-20. [张少华, 江泽飞, 宋三泰, 等. 泰索帝联合希罗达治疗蒽环类化疗失败复发转移性乳腺癌 的临床研究[J]. ]癌症进展, 2004, 2(3): 217-20. |
| [6] | Dong FL, Lv ZJ, Liu JS. The progress of different approaches of targeted treatment of tumor[J]. Xi Bao Yu Fen Zi Mian Yi Xue Za Zhi, 2003, 19(6): 623-5. [董兰凤, 吕占军, 刘京生. 肿瘤的靶向 治疗不同途径的研究进展[J]. 细胞与分子免疫学杂志, 2003, 19(6): 623-5.] |
| [7] | Gao DR, Wun ZP, Wang L, et al. The effect of sipulin in improving marrow depress and symptom induced by chemotherapy[J]. Xian Dai Zhong Liu Yi Xue, 2007, 15(2): 262-3.[高德荣, 温珍平, 王磊, 等. 斯普林治疗化疗所致骨髓抑制和改善生活质量的效果[J]. 现代肿瘤医学, 2007, 15(2): 262-3.] |
 2014, Vol. 41
2014, Vol. 41


