Effect of PD1-TCF1+CD8+ Stem-like Memory T Cells on Immunotherapy Prognosis and Tertiary Lymphoid Structures in Tumors
-
摘要:目的
探讨PD1-TCF1+CD8+干细胞样记忆T细胞在肿瘤微环境中的表达及对免疫治疗预后及三级淋巴结构(TLSs)的影响。
方法收集33例武汉大学人民医院接受免疫治疗的晚期胸部肿瘤患者病理组织切片,18例NSCLC及15例食管鳞癌(ESCC)。多重免疫荧光技术对PD1-TCF1+CD8+T细胞表型进行定量分析,Kaplan-Meier法绘制生存曲线,Pearson检验进行相关性分析。
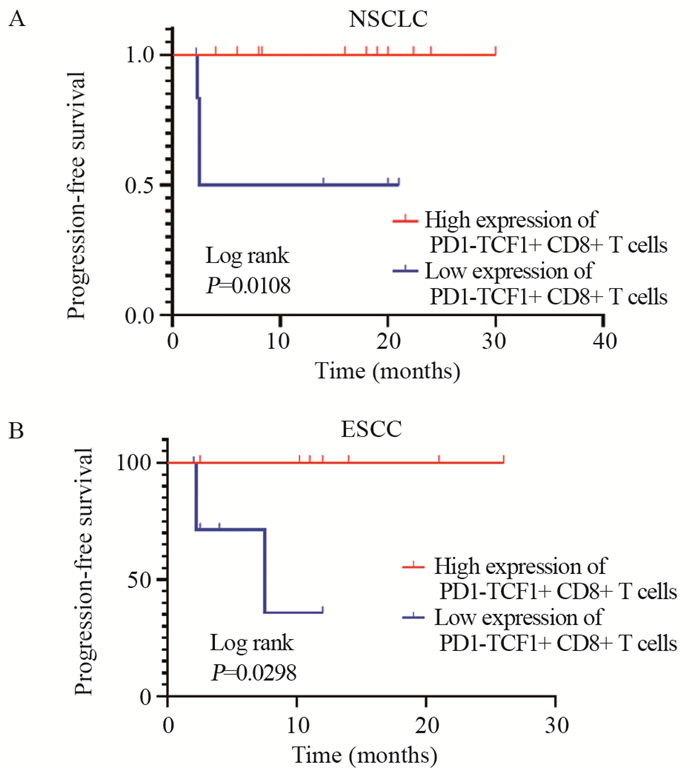
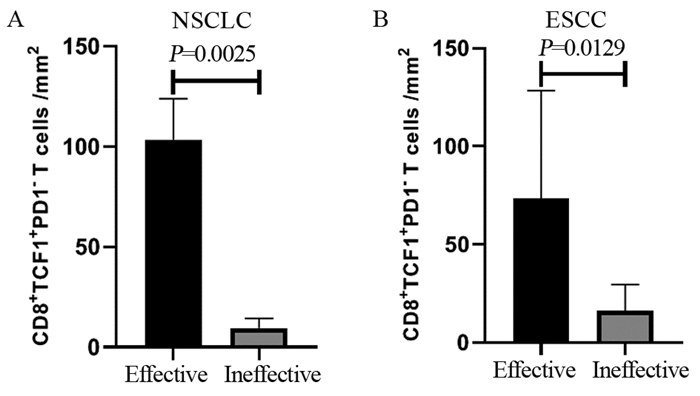
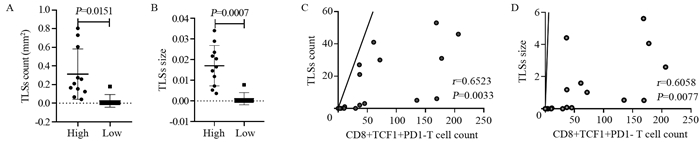
结果PD1-TCF1+CD8+T细胞的高表达与更好的无进展生存期(PFS)和免疫治疗疗效有关;在NSCLC队列中,PD1-TCF1+CD8+T细胞的高表达还与三级淋巴结构的数量(P=0.0017)及相对面积(P=0.006)显著正相关。
结论在NSCLC和ESCC患者中,PD1-TCF1+CD8+干细胞样记忆T细胞的高表达可能与良好的预后及免疫治疗疗效有关,并且在NSCLC中与肿瘤微环境内TLSs的形成密切相关。
Abstract:ObjectiveTo investigate the impact of PD1-TCF1+CD8+ stem-like memory T cells on immunotherapy prognosis and tertiary lymphoid structure in tumors.
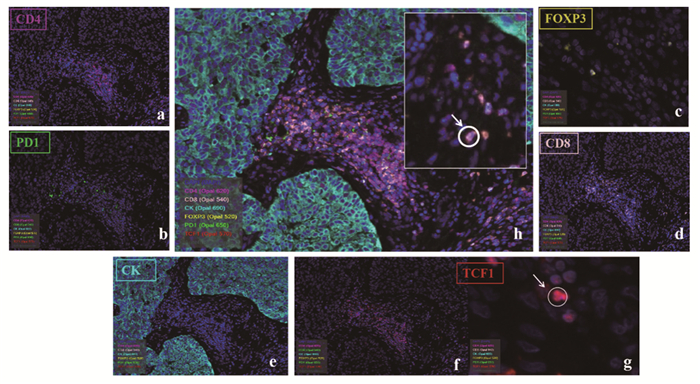
MethodsPathological tissue sections were collected from 33 patients treated with immunotherapy, 18 cases of NSCLC and 15 cases of ESCC. The expression of PD1-TCF1+CD8+T cells was detected through quantitative analysis by multiplex immunofluorescence. Survival curves were described by the Kaplan-Meier method. Pearson's correlation test was used for correlation analysis.
ResultsThe high levels of PD1-TCF1+CD8+T cells had a better PFS in NSCLC and ESCC cohorts. In the NSCLC cohort, high levels of PD1-TCF1+CD8+ T cells were significantly and positively correlated with the number (P=0.0151) and size (P=0.0007) of TLSs.
ConclusionIn patients with NSCLC and ESCCs, high PD1-TCF1+CD8+ stem-like memory T cell expression indicates improved prognosis and immune response and is associated with the formation of TLSs in the tumor microenvironment of NSCLC.
-
0 引言
结直肠癌是常见的消化系统恶性肿瘤,随着治疗手段的不断增多,患者的生存时间得到了明显延长,但肿瘤复发和耐药仍然是临床工作中面临的巨大难题。越来越多的证据表明,结直肠癌的发生、发展是转化细胞和其微环境相互作用的结果,肠癌干细胞被认为是肿瘤复发、耐药和转移的主要触发因素[1]。深入了解肠癌干细胞的调控机制、异质性、特异性标志物、信号通路以及它们与肠道微环境组分的相互联系是提高结直肠癌治疗效果的必要条件。因此,根除肠癌干细胞可能是结直肠癌新的治疗方向。
1 肠癌干细胞的特性及演变
肿瘤干细胞是肿瘤内少量的具有恶性表型特征的未分化致瘤细胞。20世纪90年代科学家证实了肿瘤干细胞的存在[2]。肿瘤干细胞不断积累突变,具有干细胞性、多药耐药、放射耐药、凋亡耐药、DNA修复等各种能力。因其具有对上皮组织进行自我更新和分化克隆等独特特征,故具有明显的异质性。
在人类结肠的每个隐窝中,只有4~6个具有无限增殖能力且能长时间存活的肠道干细胞(intestinal stem cells,ISCs),分布在肠上皮细胞中的两个不同的干细胞池:活跃的肠干细胞和储备的肠干细胞。前者位于隐窝基底膜,在完整条件下负责维持上皮内稳态,而后者能促进损伤后上皮再生。这两个细胞池可以相互转化,从而保持数量平衡。
研究发现,肠道干细胞是启动肠癌细胞重要的细胞来源。活跃的肠道干细胞使上皮细胞转换,通常由以下信号通路介导:Wnt/β-连环蛋白[3]、Ras/Raf/Mek/Erk/MAPK、Notch和BMP/Smad。APC诱导的Wnt/β-连环蛋白信号通路的激活被认为是肠道干细胞引发肠道畸形的第一步。随着P53功能的丧失,异常的ISCs数量明显增加,表现出较差的分化能力[4]。同时,当Smad4和Kras发生突变[5]时,这些细胞具有明显的侵袭性。异常的Wnt信号压倒性地驱动了肠癌细胞的发病程序。由于这些级联反应,正常的肠干细胞便转化为肠癌干细胞(cancer stem cells, CSCs)。
另一方面,结直肠黏膜的上皮细胞向间充质细胞的正常转化(EMT)可以使结直肠癌细胞获得肿瘤干细胞特征[6]。在EMT期间,紧密排列的上皮细胞转变为间充质细胞,表现为高侵袭性和运动性,在肿瘤的侵袭、进展和治疗中起着关键作用[7]。
2 肠癌干细胞标志物
CSCs可以从一个或多个细胞表面标志物的表达中被识别出来,如CD133、CD44、CD24、CD166和Lgr5[8]等。目前报道的所有CSCs标志物都在具有肿瘤起始能力[9]的结肠癌细胞上共表达。在人类前列腺、肾脏、肝细胞[10]、结肠和胰腺癌中,相比CD133-的细胞而言,少量的CD133+细胞被证明有更高的致瘤和克隆潜能。然而,大多数关于CSCs标志物在人类肿瘤中表达的争议都集中在这一最常用的标志物上。研究发现CD133+和CD133-的细胞在免疫缺陷小鼠中均能促进肿瘤生长,认为CD133不能作为转移性结肠癌CSCs的标志物,但没有证据证明CD133-群体在原发肿瘤中的肿瘤起始能力,不能表明CD133的表达在原发肿瘤中与肿瘤干细胞群体无关,有可能原发性肿瘤和转移性肿瘤的CSCs之间存在区别。因此,尽管CD133不是一个完美的标志物,但它已经是识别、富集和分离各种肿瘤CSCs的最成功的标志物之一。然而,并非所有的CSCs都具有相同的基因图谱。结直肠CSCs的一些亚群有自己的标志物,如CD26、CD110和含cub结构域的蛋白-1(CDCP-1)[11]。这些结果表明,结直肠CSCs具有不同的基因谱,这是一个反映CSCs异质性[12]的证据。
3 肿瘤微环境与肠癌干细胞的关系
在肿瘤进展过程中,基质与肿瘤细胞进行物质交换并共同发展。一方面肿瘤细胞改变基质的组成及性质,另一方面形成适应肿瘤细胞生长的微环境(tumor microenvironment, TME),还为肿瘤细胞提供保护。肿瘤微环境中的多种细胞和非细胞元素之间存在着复杂和动态的相互作用。
肿瘤微环境中包含癌相关成纤维细胞(carcinoma-associated fibroblasts, CAFs)、间质肌成纤维细胞、骨髓间充质干细胞(mesenchymal stem cells, MSCs)、树突状细胞(dendritic cell, DC)、内皮细胞、炎性反应免疫细胞和组织细胞。这些非肿瘤细胞被认为可以保护CSCs免受抗肿瘤治疗的影响。另外,肿瘤微环境中的各种成分,如细胞因子、转录因子、细胞外囊泡和自由基均互相应答,互相交叉,如TGF-β、NF-κB、IL-6、IL-8以及缺氧等因素均在调节肠癌干细胞功能方面发挥着关键作用[13]。同时,微环境中的不同成分在细胞可塑性中起着关键作用。可塑性是TME影响肿瘤复发的一个主要特征,可导致致瘤细胞和非致瘤细胞之间的可逆转变。可塑性被认为是单周期治疗不足、仅消除活跃CSCs而治疗效果不佳的一个原因[14],也叫作肿瘤干细胞的自主耐药性[15]。Garza-Treviño等[16]发现,与HCT116高密度单培养相比,在高密度微环境共培养中,HCT116干细胞标志物(CD133)的表达显著增加,说明肿瘤微环境是刺激和支持肿瘤干细胞形成的主导因素。
3.1 缺氧
缺氧,作为肿瘤微环境的一个组成部分,被认为是肿瘤进展的主调节因子和驱动力,也是CSCs/TME相互作用的主要标志。肿瘤干细胞可能位于肿瘤微环境的缺氧区,缺氧诱导因子(hypoxia inducible factor, HIF)与肿瘤干细胞的存活有关[17]。miR210是抑制DNA修复的重要调控因子,其表达受到HIF1α的直接调控,并促进常氧基因mRNA的降解。敲除miR210可抑制缺氧诱导的胶质瘤干细胞样细胞的自我更新能力和抗性。miR210和HIF1α在多种肿瘤中正相关,而miR126和HIF1α在结肠癌中显著负相关,提示它们的表达可用于肿瘤的早期诊断和筛查[18]。
研究发现,包括Wnt和Notch通路在内的肿瘤干细胞信号通路在缺氧的微环境中被激活[1]。此外,在微环境中,CSCs能表达高水平的程序性死亡配体1(programmed death ligand 1, PD-L1),该配体与程序性死亡受体1(programmed cell death protein 1, PD-1)结合抑制T细胞的功能。肿瘤干细胞还能向TME分泌多种细胞因子,如TGF-β、IL-4、IL-10和IL-13,对免疫细胞产生抑制作用,从而获得免疫逃逸[10]。
3.2 癌相关成纤维细胞
活化的成纤维细胞在肿瘤内受细胞因子和趋化因子的刺激,被称为癌相关成纤维细胞(CAFs)[19]。CAFs是肿瘤微环境中显示异质性和复杂性的主要组成部分。在肿瘤微环境中,癌相关成纤维细胞已被证明在肿瘤的发展中发挥多种作用[20]。研究表明,CAFs可分泌多种可溶性信号因子,诱导多种表型,如增强细胞增殖、改变代谢、增加细胞运动性、上调邻近肿瘤细胞的血管生成以及其他基质细胞类型的调控[21]。
CAFs能激活Hedgehog(Hh)干细胞信号通路,Hh也是肿瘤干细胞在微环境中的另一个重要的调节因子。特别是CD10+癌相关成纤维细胞,研究发现,结肠癌组织中[22],CD133+细胞和CD133-细胞分别在体内外与初级CD10成纤维细胞共同培养,与CD10-成纤维细胞相比,CD10+成纤维细胞共培养显著提高了CD133+细胞的致瘤能力和侵袭性。
3.3 微环境中EMT介导的肠癌干细胞
肿瘤微环境中的各种因素能促进上皮-间充质转化的进程,进一步诱导肿瘤干细胞形成,上皮-间充质转化可能是侵袭转移的先导机制[23]。EMT能诱导癌细胞具有侵袭和转移性,也被认为是肿瘤干细胞形成的触发因素。其过程包括下调细胞黏附分子等钙黏蛋白,同时促进N-钙黏蛋白、波形蛋白、纤维连接蛋白、锌指蛋白(SNAIL、Slug、ZEB)和基质金属蛋白酶(MMPs)的表达,引导肿瘤细胞表现出更大的细胞流动性和恶性特征。
整个EMT过程主要受到TGF-β调控。转化生长因子-β(TGF-β)是一种多功能多肽,在正常组织的分化、增殖和胚胎发育中发挥重要作用。组织细胞合成并分泌TGF-β进入微环境,与特定的受体结合,进行旁分泌和自分泌信号传递。这种配体和受体复合物刺激细胞内信号级联,包括典型的Smad2信号通路,它与Smad4形成复合物,在细胞核中调节特定基因的转录,并最终调节细胞周期和组织修复[24]。
在口腔癌中,上皮-间充质转化对于获得干细胞特性至关重要。Zubeldia[25]等用TGF-β1转染结肠癌干细胞,显示转染的细胞具有α-平滑肌肌动蛋白的强信号,该肌动蛋白是EMT表型的标志物。Kim等[26]发现TGF-β1能诱导结肠癌中Twist1的激活,在淋巴结转移的样本中TGF-β1的表达较高,TGF-β1 mRNA的表达与Twist1正相关,而Twist正是上皮-间充质转化过程中的调节因子,在乳腺癌、前列腺癌和皮肤癌中高表达。
3.4 炎性反应免疫细胞
炎性反应免疫细胞如单核细胞、巨噬细胞、中性粒细胞和淋巴细胞是肿瘤微环境中的细胞成分。炎性反应免疫细胞由CAFs和癌细胞分泌的趋化因子和细胞因子所招募。大量证据表明,阿司匹林(环氧化酶抑制剂)和其他传统的非甾体抗炎药可以降低结肠癌发生转移的风险[27]。炎性肠病与结肠癌的关系可能是微环境中炎性反应对细胞的刺激作用所致[28]。炎性肠病中持续的黏膜炎性反应和其他相关因素,如黏膜破裂和肠道微生物群,可促进胃肠道的细胞变化为癌前细胞,并最终形成肠癌干细胞,其机制可能是COX酶通过抑制β-连环蛋白降解驱动前列腺素E2,并作为介导Wnt通路的信号。
3.5 微环境中的血管生成
CSCs的自我更新和肿瘤的启动伴随着促血管生成因子的分泌如血管内皮生长因子(vascular endothelial growth factor,VEGF)[29]来促进血管生成。研究发现经结肠癌干细胞预处理的SW480细胞培养后,能增强HUVEC管的形成,VEGFA表达明显升高[30]。使用TGF-β1干预结肠癌干细胞在体外显示出更高的血管密度,而小鼠转染这些TGF-β1阳性细胞导致内皮细胞和循环内皮祖细胞高表达,表明TGF-β1诱导血管生成[31]。这些证据表明,TGF-β在结肠癌干细胞血管生成的起始过程中起着关键作用。
4 肿瘤微环境靶向治疗策略
目前肠癌干细胞被认为是治疗耐药性和肿瘤复发的主要原因,了解肿瘤微环境中肿瘤干细胞和其他成分之间的联系,可能是抑制CSCs生长潜能的一个重要治疗靶点。因此,为了制定新的肠癌治疗策略,有必要更详细地研究肠癌干细胞与微环境中各个成分的相互作用,以阐明其发生发展的详细机制。
4.1 上皮细胞向间充质细胞转化的阻断
EMT不仅能诱导癌细胞获得侵袭性和转移性,还能使癌细胞获得耐药性,使治疗方法复杂化。其根本机制是触发了结肠癌干细胞的逆转,或使休眠干细胞转为活跃,这可能就是EMT、CSCs和耐药性之间的关联。靶向EMT通路可能是一种很有前途的治疗策略。Qi等[32]已经证明了Dickkopf-1(Dkk1)可以作为一种Wnt信号抑制剂逆转结肠癌中的EMT。在217例结肠癌患者中,发现Dkk1的表达与肿瘤分期、转移和复发负相关;Dkk1阳性样本比阴性样本能更高地表达上皮标记E-钙黏蛋白,降低间充质标记波形蛋白和细胞质分布,表明Dkk1在结肠癌可能减少间充质化,能使EMT过程逆转,因此可作为肿瘤治疗的靶点。
4.2 调控癌相关成纤维细胞
TGF-β、Hh等多个信号通路参与不同来源细胞的CAF激活,靶向这些信号通路可能是调控癌相关成纤维细胞的重要途径。TGF-β被认为是CAF分化、激活和扩张的主要中介物。TGF-β及其家族成员激活TGF-βR1受体,而TGF-βR1受体进而磷酸化Smad2/3,形成核易位的Smad2/3/4复合物,这些复合物通过与转录因子、共激活因子等信号通路合作,负责靶基因的表达。另外,癌相关成纤维细胞不仅可以分泌多种细胞因子或代谢产物抑制免疫细胞的功能,还能塑造肿瘤外基质,形成药物或免疫细胞渗透屏障,阻止药物和免疫细胞向肿瘤组织渗透。Colangelo等[33]报道使用抗纤维化药物或多靶向药物可使CAFs逆转为正常成纤维细胞。通过调控癌相关成纤维细胞或克服其屏障作用可能是肿瘤治疗的新手段。
4.3 微环境中血管生成的干预
证据表明,肠癌干细胞可直接分化为血管内皮细胞,从而产生肿瘤所需的血管系统。异常的血管系统能够阻碍肿瘤的免疫反应以及氧气和化疗药物的运输和分配,这种恶劣的肿瘤微环境也可以导致对放化疗耐药[34]。另一方面,抗血管生成药物易诱导肿瘤缺氧,使CSCs存活和传播,从而推动肿瘤进展,所以目前临床上使用的VEGF靶向药物对肿瘤患者的生存获益有限。由于CSCs是微环境中VEGF的主要来源,因此特异性地靶向CSCs或干细胞来源的VEGF可能是有效的。可见,更好地了解CSCs与肿瘤血管生成之间的关系是研究血管生成靶向药物的新途径。
4.4 天然植物化学物质作为CSCs靶向的抗癌药物
近年来,一些天然植物化学物质,比如姜黄素、白藜芦醇、环巴胺、胡椒碱等均被报道能针对肠癌干细胞的活性。Sankpal等[35]研究发现姜黄素通过影响核因子κB(NF-κB)进入细胞核,抑制微环境中成纤维细胞和结肠CSCs之间的连接,并使肠癌干细胞对5-Fu敏感。白藜芦醇是一种多酚类化合物,存在于许多植物物种中,如葡萄、花生和浆果中[36],研究发现其对胰腺癌干细胞和胰腺癌细胞的迁移、侵袭和上皮-间充质转化均有潜在的抑制作用。因此,开发天然植物化学物质并探讨其作用机制,是针对肿瘤干细胞治疗的另一重要途径。
5 结语
结直肠癌的生长、复发和转移可能取决于肿瘤干细胞及其微环境,肿瘤干细胞需要与微环境相互作用才能生存,微环境的组成可能影响患者对治疗的反应,因此,结直肠癌的治疗不仅要针对肠癌干细胞,还需要针对肿瘤微环境及其成分,但肿瘤微环境中的各种细胞和非细胞成分间存在着复杂的动态平衡,深入了解其作用机制,寻找合适的生物标志物,如何通过精准靶向来提高结直肠癌的疗效是我们面临的一个重大挑战。
Competing interests: The authors declare that they have no competing interests.作者贡献:崔雪:试验设计、基础实验及数据统计、撰写及修改论文翁一鸣:试验指导王培伟:临床资料收集彭敏:指导试验设计、修改论文 -
表 1 多重免疫荧光试剂盒及试剂信息
Table 1 Multiplex IHC KIT

表 2 多重免疫荧光抗体组合的设计
Table 2 Design for multiplex IHC antibody panel

-
[1] Ribas A, Wolchok JD. Cancer immunotherapy using checkpoint blockade[J]. Science, 2018, 359(6382): 1350-1355. doi: 10.1126/science.aar4060
[2] Wherry EJ. T cell exhaustion[J]. Nat Immunol, 2011, 12(6): 492-499. doi: 10.1038/ni.2035
[3] Blank CU, Haining WN, Held W, et al. Defining 'T cell exhaustion'[J]. Nat Rev Immunol, 2019, 19(11): 665-674. doi: 10.1038/s41577-019-0221-9
[4] Kim C, Jin J, Weyand CM, et al. The Transcription Factor TCF1 in T Cell Differentiation and Aging[J]. Int J Mol Sci, 2020, 21(18): 6497. doi: 10.3390/ijms21186497
[5] Steinke FC, Xue H. From inception to output, Tcf1 and Lef1 safeguard development of T cells and innate immune cells[J]. Immunol Res, 2014, 59(1-3): 45-55. doi: 10.1007/s12026-014-8545-9
[6] Zhao X, Shan Q, Xue HH. TCF1 in T cell immunity: a broadened frontier[J]. Nat Rev Immunol, 2022, 22(3): 147-157. doi: 10.1038/s41577-021-00563-6
[7] Galletti G, De Simone G, Mazza EMC, et al. Two subsets of stem-like CD8+ memory T cell progenitors with distinct fate commitments in humans[J]. Nat Immunol, 2020, 21(12): 1552-1562. doi: 10.1038/s41590-020-0791-5
[8] Seo W, Jerin C, Nishikawa H. Transcriptional regulatory network for the establishment of CD8+ T cell exhaustion[J]. Exp Mol Med, 2021, 53(2): 202-209. doi: 10.1038/s12276-021-00568-0
[9] Pimenta EM, Barnes BJ. Role of Tertiary Lymphoid Structures (TLS) in Anti-Tumor Immunity: Potential Tumor-Induced Cytokines/Chemokines that Regulate TLS Formation in Epithelial-Derived Cancers[J]. Cancers (Basel), 2014, 6(2): 969-997. doi: 10.3390/cancers6020969
[10] Romero D. B cells and TLSs facilitate a response to ICI[J]. Nat Rev Clin Oncol, 2020, 17(4): 195. doi: 10.1038/s41571-020-0338-6
[11] Ng SB, Fan S, Choo SN, et al. Quantitative Analysis of a Multiplexed Immunofluorescence Panel in T-Cell Lymphoma[J]. SLAS Technol, 2018, 23(3): 252-258. doi: 10.1177/2472630317747197
[12] Henning AN, Roychoudhuri R, Restifo NP. Epigenetic control of CD8(+) T cell differentiation[J]. Nat Rev Immunol, 2018, 18(5): 340-356. doi: 10.1038/nri.2017.146
[13] Wen S, Lu H, Wang D, et al. TCF-1 maintains CD8(+) T cell stemness in tumor microenvironment[J]. J Leukoc Biol, 2021, 110(3): 585-590. doi: 10.1002/JLB.5MR1120-778R
[14] Harly C, Kenney D, Ren G, et al. The transcription factor TCF-1 enforces commitment to the innate lymphoid cell lineage[J]. Nat Immunol, 2019, 20(9): 1150-1160. doi: 10.1038/s41590-019-0445-7
[15] Zhang J, Lyu T, Cao Y, et al. Role of TCF-1 in differentiation, exhaustion, and memory of CD8+ T cells: A review[J]. FASEB J, 2021, 35(5): e21549.
[16] Martin MD, Badovinac VP. Defining Memory CD8 T Cell[J]. Front Immunol, 2018, 9: 2692. doi: 10.3389/fimmu.2018.02692
[17] Kanev K, Zehn D. Origin and fine-tuning of effector CD8 T cell subpopulations in chronic infection[J]. Curr Opin Virol, 2021, 46: 27-35. doi: 10.1016/j.coviro.2020.10.003
[18] Dieu-Nosjean MC. Tumor-Associated Tertiary Lymphoid Structures: A Cancer Biomarker and a Target for Next-generation Immunotherapy[J]. Adv Exp Med Biol, 2021, 1329: 51-68.
[19] Cabrita R, Lauss M, Sanna A, et al. Tertiary lymphoid structures improve immunotherapy and survival in melanoma[J]. Nature, 2020, 577(7791): 561-565. doi: 10.1038/s41586-019-1914-8
[20] Sautes-Fridman C, Petitprez F, Calderaro J, et al. Tertiary lymphoid structures in the era of cancer immunotherapy[J]. Nat Rev Cancer, 2019, 19(6): 307-325. doi: 10.1038/s41568-019-0144-6
-
期刊类型引用(2)
1. 黄芸,陈文俊,朱伟敏,王峰. 2015—2022年克拉玛依市消化系统恶性肿瘤死亡特征与灰色模型预测分析. 疾病预防控制通报. 2024(05): 42-46+56 .  百度学术
百度学术
2. 王红英,李胜,明娟,李洁,李元林,杨勇攀,宋启瑞. 2006—2020年中国居民胃癌死亡趋势分析——基于年龄-时期-出生队列模型. 卫生经济研究. 2023(11): 43-48 .  百度学术
百度学术
其他类型引用(0)



 下载:
下载: