Prophylactic Dexamethasone on Pain Flare in Spine Metastasis Stereotactic Body Radiotherapy and Hypofractionated Radiotherapy
-
摘要:目的
探讨椎体转移立体定向放疗(SBRT)或大分割放疗(HF)疼痛爆发(PF)的发生率及地塞米松在预防疼痛爆发中的作用。
方法行椎体转移SBRT治疗的65例患者随机分为对照组(32例,仅行SBRT或大分割放疗)和治疗组(33例,行SBRT或大分割放疗同时给予4.5 mg地塞米松治疗)。简明疼痛量表(BPI)用来评估治疗前、治疗过程中和治疗后患者疼痛评分。记录每组患者疼痛爆发情况,比较两组患者PF发生率。
结果全组患者发生PF为24.6%,对照组发生率为37.5%例,治疗组发生率为12.1%例,两组PF比较差异有统计学意义(P=0.018)。两组患者PF主要发生在d1~2,占整个PF的62.5%,其中对照组为66.7%,治疗组为50%,在d1~2发生PF两组比较差异无统计学意义(P=0.551)。比较不同分次方案与PF关系,对照组3F与10F中PF发生率分别为66.7%和33.3%(P=0.001)。治疗组3F与10F中PF发生率分别为50%和50%(P=0.643)。
结论口服地塞米松在预防和治疗椎体转移SBRT或HF的PF具有较好的疗效,显著降低PF发生率。
Abstract:ObjectiveTo explore the incidence of pain flare (PF) in spine metastasis stereotactic body radiotherapy (SBRT) or hypofractionated radiotherapy (HF) and the prophylactical effect of dexamethasone.
MethodsSixty-five patients were treated with spine metastasis SBRT and randomly divided into control group (SBRT or HF, n=32) and treatment group (SBRT or HF and 4.5 mg dexamethasone, n=33). The brief pain inventory (BPI) was used to score the pain before, during and after treatment. PF was recorded and compared between two groups.
ResultsThe incidence of PF was 24.6% in all patients (control group: 37.5%, treatment group: 12.1%, P=0.018). PF in both group occurred in d1-2, accounting for 62.5% in all PF (control group: 66.7%, treatment group: 50%, P=0.551). The incidences of PF in control group were 66.7% and 33.3% for three and ten fractions scheme, respectively (P=0.001). However, the incidences of PF in treatment group were 50% and 50% for three and ten fractions scheme, respectively (P=0.643).
ConclusionOral dexamethasone has an excellent efficacy in prevention and treatment of PF in spine metastasis SBRT or HF, with significantly decreased incidence of PF. A phase Ⅲ clinical trial is required to finalize the optimal dose and schedule.
-
Key words:
- Dexamethasone /
- Spine metastasis /
- Stereotactic body radiation therapy /
- Pain flare
-
0 引言
立体定向放射治疗(stereotactic body radiotherapy, SBRT)和大分割放疗(hypofractionated radiotherapy, HF)是恶性肿瘤椎体转移治疗的主要方式,利用SBRT剂量迅速跌落的优势形成陡峭的剂量曲线,给予肿瘤区域较高的照射剂量,而同时对周围正常组织,尤其是脊髓部产生严重的损伤。临床研究已经证实SBRT可以提高疼痛控制和肿瘤局部控制[1-2]。SBRT潜在的晚期不良反应包括放射性脊髓炎和压缩性骨折,急性不良反应包括疼痛爆发(pain flare, PF)[3-4]。一些相关研究表明SBRT后PF的发生率可达到23%~68%[5-7]。初步研究结果表明,影响PF的因素包括KPS、病变椎体位置、分次剂量和治疗前没有进行甾体类药物预防[6-7]。地塞米松可以缓解及预防PF[7],然而,地塞米松在预防PF时的剂量、使用时间、在不同分割方案中的作用临床相关研究较少。因此,本研究目的是明确地塞米松在椎体转移SBRT或HF中减少PF发生中的作用。
1 资料与方法
1.1 研究对象
收集2016年10月—2019年10月行椎体转移SBRT的65例患者,转移病灶79个,随机分为观察组和治疗组。对照组32例仅行SBRT或HF,治疗组33例行SBRT或HF同时给予4.5 mg地塞米松治疗。入组患者同期可以进行止痛药物治疗、靶向或免疫治疗,未进行系统化疗和其他部位放疗。所有患者治疗前均伴有局部疼痛,男45例、女20例,平均年龄55岁。原发病变主要为肺癌、乳腺癌、肾癌、结直肠癌、肝癌及食管癌,转移部位颈椎5例,胸椎39例,腰骶椎21例,见表 1。所有患者KPS评分≥60分,预期生存 > 6月。
表 1 两组患者入组特征Table 1 Clinical characteristic of included patients
1.2 治疗方案
根据CT和MRI的融合图像勾画肿瘤区和脊髓。临床靶区根据国际SRS协作组指南(International Spine Radiosurgery Consortium, ISRCC)靶区勾画指南进行勾画[5]。处方剂量为27 Gy/3 F或45~48 Gy/10 F。24例行sIMRT,计划设计采用Pinnacle 9.6版本计划系统,采用单中心、共面、11野计划设计。放疗设备为医科达Varian直线加速器及CBCT进行图像引导。39例行VMAT,放疗设备为Varian RapidArc直线加速器。A组仅行SBRT或HF;B组行SBRT或HF同时给予地塞米松治疗,具体方案采用上午放疗,放疗前1 h口服地塞米松4.5 mg,对于3次的SBRT,而后d1、d2、d3、d4早上继续口服相同剂量的地塞米松,对于10 F的HF要服药至少到d5。对于一些激素使用禁忌证的患者,不包括在此研究中。
1.3 疼痛评估
疼痛爆发定义:在未减少止痛药物剂量的前提下疼痛评分在基线水平上增加两点,或者疼痛评分没有变化的前提下增加了25%的止痛药物剂。NRPS(Numerical evaluation pain score)是一个简单的疼痛测量量表,0~10分共11个层级,用来记录患者疼痛情况。记录每组患者疼痛爆发情况。
1.4 治疗疗效评价
患者将完成NRPS表,记录脊柱转移瘤最严重的疼痛,包括基线临床随访(治疗当天),及治疗后在家1,2,3周后4个时间点,并记录止痛药的使用和不良反应。疗效评价分为:(1)完全缓解疼痛:指在治疗后3月疼痛评分为0,完全缓解疼痛是基于没有增加止痛药;(2)部分缓解疼痛:只要没有其他病变治疗增加了疼痛分数,只要患者不需要增加麻醉止痛药的水平,NRPS减少≥3(即从基线开始NRPS至少减少3分);(3)反应稳定:在没有增加麻醉止痛药的情况下,患者治疗后疼痛减少2分以内;(4)疾病进展:指治疗后疼痛增加至少3分。
1.5 统计学方法
采用SPSS22.0软件进行统计分析,计量资料以均数±标准差表示,局部控制和生存数据分析采用Kaplan-Meier检验,入组患者特征连续变量采用秩和检验,分类变量采用χ2检验。P < 0.05为差异有统计学意义。
2 结果
两组患者入组特征见表 1,两组患者临床特征比较差异无统计学意义。
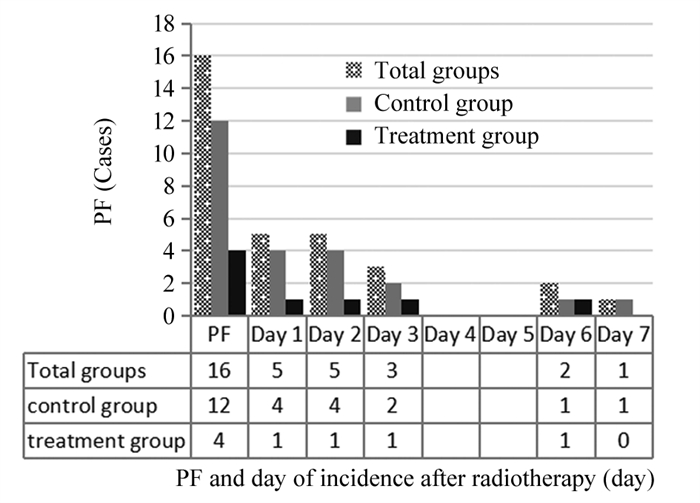
全组患者发生PF为24.6%(16/65),其中对照组发生率为37.5%(12/32),治疗组发生率为12.1%(4/33),给予地塞米松预防及治疗后PF发生率显著下降,两组PF比较差异有统计学意义(χ2=5.639, P=0.018),见图 1。两组PF主要发生在d1~2,占整个PF的62.5%(10/16),其中对照组为66.7%(8/12),治疗组为50%(2/4),在d1~2发生PF两组比较差异无统计学意义(χ2=0.356, P=0.551)。在PF患者中,发生轻度疼痛(1~4级)37.5%(6/16),中度疼痛(5~6级)43.8%(7/16),重度疼痛(7~10级)25%(18.7/16),对照组与治疗组比较,轻度疼痛(5 vs. 1, P=0.551)、中度疼痛(5 vs. 2, P=0.771)和重度疼痛(3 vs. 1, P=1.000)间差异无统计学意义。
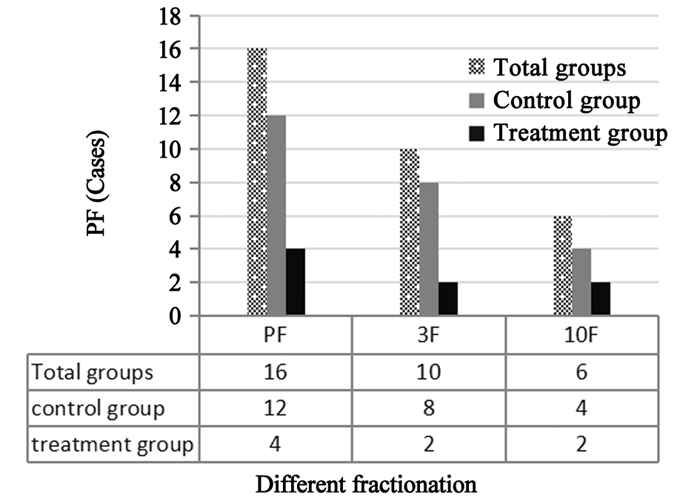
关于不同分次方案与PF关系,见图 2。对照组中3F方案为66.7%(8/12),10F方案为33.3%(4/12),两组比较PF发生率差异有统计学意义(χ2=11.210, P=0.001)。治疗组中3F方案为50%(2/4),10F方案为50%(2/4),两组比较PF发生率差异无统计学意义(χ2=0.214, P=0.643)。
放疗结束后4周,全组患者疼痛缓解率89.2%(58/65)。6月和1年局部控制率分别为87.7%和84.6%。中位随访11月(6~42月),全组患者中位生存31月,6月和1年总生存分别为90.7%和85.9%。晚期损伤椎体压缩性骨折发生率1.5%(1/65),无其他晚期不良反应。
3 讨论
常规放射治疗是恶性肿瘤椎体转移主要治疗方式,但其症状缓解率和局部控制率相对较低,平均症状缓解率达70%,中位缓解时间仅为3~7月[8],靶区处方剂量过低是患者症状不能缓解和治疗失败的主要因素[9-11]。随着免疫治疗和靶向治疗在临床中应用越来越广泛,在椎体转移方面尽早进行SBRT可以缓解患者症状、提高局部控制并改善生存[12],Miller等报道肾癌椎体转移SBRT同步TKI治疗,椎体局部复发率为4%,显著低于先行TKI再行SBRT(19%~27%)[13]。
SBRT在椎体转移瘤治疗中的优势在于给予肿瘤靶区高剂量的同时,可以有效地保护周围的正常组织,尤其是脊髓,在椎体转移瘤放疗中应用越来越广泛。一项关于SBRT临床应用的调查显示,67.5%的被调查单位椎体转移瘤应用SBRT位列第二位[14]。研究报道SBRT潜在的急性不良反应主要为PF,发生率可达23%~68%[5-7]。如何减少PF的发生,对椎体转移SBRT患者保证治疗过程中体位的稳定性和重复性、保证整个治疗过程精确实施并提高患者生活质量至关重要。
PF定义为在未减少止痛药物剂量的前提下疼痛评分在基线水平上增加两点,或者疼痛评分没有变化的前提下增加了25%的止痛药物剂量[3, 15]。PF是椎体转移瘤SBRT常见的不良反应,其发生率为23%~68%[5-7],明显高于常规放疗的2%~40%[3, 16],可能的机制为放射治疗导致骨膜水肿压迫及炎性因子释放引起的疼痛加重。本研究结果表明,全组患者PF发生率为24.6%(16/65),比文献报道的结果偏低,可能与入组患者有关,我们选择的全部患者在治疗前均有不同程度的疼痛,可能部分患者对疼痛发生耐受,对出现的轻度PF没有作出很好的评价。
对于椎体转移SBRT后出现的PF,相关研究初步认为预防给予地塞米松可以减低疼痛爆发的发生。Khan等[15]报道给予口服地塞米松预防后,47例患者中19%出现PF,而没有给予预防的PF发生率为68%,给予地塞米松预防后降低49%的PF发生率。目前有研究也在开展关于如何进行预防和治疗PF。van der Linden和Westhoff等[5, 17]开展Ⅲ期临床研究,入组295例患者,采用随机对照、双盲多中心研究,入组患者放疗前一天口服地塞米松或安慰剂,放疗后连用3天。入组患者分为三组:A组为口服8 mg地塞米松组;B组为放疗前口服8 mg地塞米松,放疗后3天使用安慰剂;C组为安慰剂组。其评价终点为PF发生率。研究结果显示地塞米松没有显著减少PF发生率,但可以延迟PF发生率并在第2~5天降低平均疼痛评分。Khan等[15]也进行相关研究,比较地塞米松不同剂量在PF中的疗效。47例患者分为两组,A组在治疗前1 h给予地塞米松4 mg,d2~4连用;B组在治疗前1 h给予地塞米松8 mg,d2~4连用。研究结果表明,全组患者PF发生率19%,A组患者为25%,两组患者为13%,两组疗效差异无统计学意义(P=0.46),但在运动能力改善方面A组(4 mg组)更有优势(P < 0.005)。Chow等[18]开展的骨转移放射治疗PF的Ⅲ期临床研究中,地塞米松试验组PF发生率为26%,而安慰剂组PF发生率为35%,证明地塞米松在预防放疗引起的PF方面具有显著性疗效(P=0.03)。基于以上研究,本研究方案采用提前预防的4.5 mg地塞米松治疗方案,因为地塞米松的半衰期是36~54 h,提前预防使用可能会更好的改善PF,结果表明在SBRT前1天、第1~5天给予地塞米松显著降低PF发生率,由未给予预防37.5%降低到给予预防12.1%(P=0.018)。
Pan等[11]的研究表明,SBRT分割次数与疼痛爆发具有相关性:单分次、3分次和5分次SBRT的疼痛爆发发生率分别为34%、20%和8%(P=0.005)。分割次数也是疼痛爆发的独立预后因素。有研究表明PF与分割剂量及照射次数无相关性[5-7, 19]。本研究结果表明,在对照组3F和10F的PF发生率差异有统计学意义(66.7% vs. 33.3%, P=0.001),而在试验组3F和10F的PF发生率差异无统计学意义(50% vs. 50%, P=0.643)。提示PF发生率与照射次数和照射剂量相关,给予地塞米松预防后可能减少PF发生率,但由于研究样本量相对较少,有待进一步研究证实。
地塞米松具有治疗骨转移引起的疼痛爆发作用,与止痛药物联合具有协同作用,另外地塞米松也可以减少治疗相关的恶心和呕吐,保证放疗的顺利完成。研究显示椎体转移SBRT患者给予地塞米松显著降低PF发生率,短期使用4.5 mg地塞米松并没有明显出现药物相关不良反应,如口干、乏力、软弱、精神症状等[15]。所有治疗患者采取上午治疗,治疗前1 h口服药物,避免由于服用地塞米松后兴奋及欣快感等影响睡眠。
总之,基于研究表明,地塞米松在预防和治疗椎体转移SBRT或HF中发生的PF具有较好的疗效,显著降低PF发生率,需要扩大样本量进一步研究。关于更加优化的剂量及方案尚待进一步的Ⅲ期临床研究。
Competing interests: The authors declare that they have no competing interests.作者贡献:王润梅、玉荣:撰写及修改文章杨昊:研究设计,文章撰写和修改王振飞、武瑜、李红、胡月:数据收集及统计分析 -
表 1 两组患者入组特征
Table 1 Clinical characteristic of included patients

-
[1] Glicksman RM, Tjong MC, Neves-Junior WFP, et al. Stereotactic Ablative Radiotherapy for the Management of Spinal Metastases: A Review[J]. JAMA Oncol, 2020, 6(4): 567-577. doi: 10.1001/jamaoncol.2019.5351
[2] Sohn S, Chung CK, Sohn MJ, et al. Radiosurgery Compared with External Radiation Therapy as a Primary Treatment in Spine Metastasis from Hepatocellular Carcinoma: A Multicenter, Matched-Pair Study[J]. J Korean Neurosurg Soc, 2016, 59(1): 37-43. http://europepmc.org/abstract/med/24792488
[3] Chow E, Ling A, Davis L, et al. Pain flare following external beam radiotherapy and meaningful change in pain scores in the treatment of bone metastases[J]. Radiother Oncol, 2005, 75(1): 64-69. doi: 10.1016/j.radonc.2004.12.016
[4] Pielkenrood BJ, van der Velden JM, van der Linden YM, et al. Pain response after stereotactic body radiation therapy versus conventional radiotherapy in patients with bone metastases-a phase Ⅱ, randomized controlled trial within a prospective cohort[J]. Int J Radiat Oncol Biol Phys, 2021, 110(2): 358-367. doi: 10.1016/j.ijrobp.2020.11.060
[5] van der Linden YM, Westhoff PG, Stellato RK, et al. Dexamethasone for the Prevention of a Pain Flare After Palliative Radiation Therapy for Painful Bone Metastases: The Multicenter Double-Blind Placebo-Controlled 3-Armed Randomized Dutch DEXA Study[J]. Int J Radiat Oncol Biol Phys, 2020, 108(3): 546-553. doi: 10.1016/j.ijrobp.2020.05.007
[6] Loi M, Klass ND, De Vries KC, et al. Pain flare, complexity and analgesia in bone oligometastases treated with stereotactic body radiation therapy[J]. Eur J Cancer Care (Engl), 2018, 27(6): e12915. doi: 10.1111/ecc.12915
[7] Chiang A, Zeng L, Zhang L, et al. Pain flare is a common adverse event in steroid-naive patients after spine stereotactic body radiation therapy: a prospective clinical trial[J]. Int J Radiat Oncol Biol Phys, 2013, 86(4): 638-642. doi: 10.1016/j.ijrobp.2013.03.022
[8] Guckenberger M, Sweeney RA, Hawkins M, et al. Dose-intensified hypofractionated stereotactic body radiation therapy for painful spinal metastases: Results of a phase 2 study[J]. Cancer, 2018, 124(9): 2001-2009. doi: 10.1002/cncr.31294
[9] Sahgal A, Myrehaug SD, Siva S, et al. Stereotactic body radiotherapy versus conventional external beam radiotherapy in patients with painful spinal metastases: an open-label, multicentre, randomised, controlled, phase 2/3 trial[J]. Lancet Oncol, 2021, 22(7): 1023-1033. doi: 10.1016/S1470-2045(21)00196-0
[10] Bishop AJ, Tao R, Rebueno NC, et al. Outcomes for Spine Stereotactic Body Radiation Therapy and an Analysis of Predictors of Local Recurrence[J]. Int J Radiat Oncol Biol Phys, 2015, 92(5): 1016-1026. doi: 10.1016/j.ijrobp.2015.03.037
[11] Pan HY, Allen PK, Wang XS, et al. Incidence and predictive factors of pain flare after spine stereotactic body radiation therapy: secondary analysis of phase 1/2 trials[J]. Int J Radiat Oncol Biol Phys, 2014, 90(4): 870-876. doi: 10.1016/j.ijrobp.2014.07.037
[12] Fareed MM, Pike LRG, Bang A, et al. Palliative Radiation Therapy for Vertebral Metastases and Metastatic Cord Compression in Patients Treated With Anti-PD-1 Therapy[J]. Front Oncol, 2019, 9: 199. doi: 10.3389/fonc.2019.00199
[13] Miller JA, Balagamwala EH, Angelov L, et al. Spine stereotactic radiosurgery with concurrent tyrosine kinase inhibitors for metastatic renal cell carcinoma[J]. J Neurosurg Spine, 2016, 25(6): 766-774. doi: 10.3171/2016.4.SPINE16229
[14] Pan H, Simpson DR, Mell LK, et al. A survey of stereotactic body radiotherapy use in the United States[J]. Cancer, 2011, 117(19): 4566-4572. doi: 10.1002/cncr.26067
[15] Khan L, Chiang A, Zhang L, et al. Prophylactic dexamethasone effectively reduces the incidence of pain flare following spine stereotactic body radiotherapy (SBRT): a prospective observational study[J]. Support Care Cancer, 2015, 23(10): 2937-2943. doi: 10.1007/s00520-015-2659-z
[16] Hird A, Zhang L, Holt T, et al. Dexamethasone for the prophylaxis of radiation-induced pain flare after palliative radiotherapy for symptomatic bone metastases: a phase Ⅱ study[J]. Clin Oncol (R Coll Radiol), 2009, 21(4): 329-335. doi: 10.1016/j.clon.2008.12.010
[17] Westhoff PG, de Graeff A, Geerling JI, et al. Dexamethasone for the prevention of a pain flare after palliative radiotherapy for painful bone metastases: a multicenter double-blind placebo-controlled randomized trial[J]. BMC Cancer, 2014, 14: 347. doi: 10.1186/1471-2407-14-347
[18] Chow E, Meyer RM, Ding K, et al. Dexamethasone in the prophylaxis of radiation-induced pain flare after palliative radiotherapy for bone metastases: a double-blind, randomised placebo-controlled, phase 3 trial[J]. Lancet Oncol, 2015, 16(15): 1463-1472. doi: 10.1016/S1470-2045(15)00199-0
[19] Hird A, Chow E, Zhang L, et al. Determining the incidence of pain flare following palliative radiotherapy for symptomatic bone metastases: results from three canadian cancer centers[J]. Int J Radiat Oncol Biol Phys, 2009, 75(1): 193-197. doi: 10.1016/j.ijrobp.2008.10.044
-
期刊类型引用(1)
1. 黄佳夫,张静,张蓓,徐敏. 穴位注射联合地塞米松治疗恶性肿瘤放疗相关恶心呕吐的临床效果. 临床合理用药杂志. 2022(29): 71-74 .  百度学术
百度学术
其他类型引用(0)



 下载:
下载: