-
摘要:目的
探讨信号转导与转录激活因子1(STAT1)对胶质瘤细胞系U251细胞周期的影响及其机制。
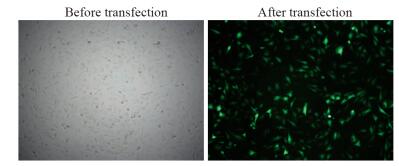
方法利用LipofectamineTM2000转染试剂体外瞬时将pcDNA3.1-STAT1转染入胶质瘤细胞系U251,将细胞分为Mock组(无转染)、空载组(转染pcDNA3.1)和STAT1组(转染pcDNA3.1-STAT1),采用Western blot法检测胶质瘤U251细胞中STAT1表达水平,MTT法检测转染STAT1的U251细胞增殖活性,流式细胞仪检测细胞周期指标,划痕实验检测细胞迁移指标,通过Western blot法检测转染细胞中P53、P21、bcl-2、Caspase-8的表达水平及变化趋势。
结果与Mock和空载组相比,STAT1组中STAT1蛋白表达量明显增高(P < 0.05),细胞增殖明显减慢(P < 0.05),G0/G1期细胞比例明显升高,细胞的迁移能力明显下降;P53、P21、Caspase-8表达明显增强(P < 0.05),bcl-2表达明显减弱(P < 0.05)。
结论高表达的STAT1对人脑胶质瘤U251细胞具有抑制增殖或促进凋亡的作用,并且STAT1可调控多分子信号转导通路,对脑胶质瘤的发生和发展起到了关键的作用。
Abstract:ObjectiveTo investigate the effect of signal transducer and activator of transcription 1 (STAT1) on cell cycle of glioma U251 cells and related mechanism.
MethodsWe transiently transfected glioma cell U251 cells with pcDNA3.1-STAT1 using LipofectamineTM2000 transfection reagent. The cells were divided into Mock group (no transfection), empty vector group (transfected with pcDNA3.1) and STAT1 group (transfected with pcDNA3.1-STAT1). The expression of STAT1 in glioma U251 cells was detected by Western blot. Cell proliferation was detected by MTT. Cell cycle was detected by flow cytometry. Wound healing assay was used to detect cell migration. The expression of P53, P21, bcl-2 and Caspase-8 in transfected cells was detected by Western blot.
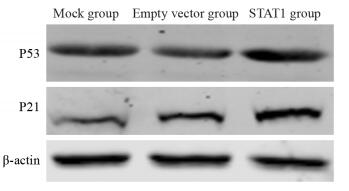
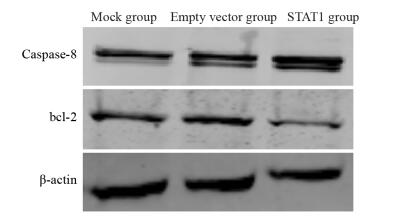
ResultsCompared with Mock group and empty vector group, the expression of STAT1 protein in STAT1 group was significantly increased (P < 0.05), cell proliferation decreased significantly (P < 0.05), the percentage of cells in phase G0/G1 increased significantly, and cell migration ability decreased significantly. The expression levels of P53, P21 and Caspase-8 increased significantly (P < 0.05) while bcl-2 decreased significantly (P < 0.05).
ConclusionThe high expression of STAT1 could inhibit the proliferation and promote the apoptosis of human glioma U251 cells, and STAT1 could regulate the expression of multiple signal transduction molecules. STAT1 plays a key role in the occurrence and development of glioma.
-
Key words:
- Glioma /
- U251 cells /
- STAT1 /
- Cell cycle /
- Apoptosis
-
0 引言
骨肉瘤(osteosarcoma)是骨科最常见的恶性肿瘤[1],其发生、发展是一个复杂的、涉及多基因调控网络失衡导致的细胞异常代谢的结果。基因表达受转录水平及翻译水平的调控,转录因子(transcription factors, TFs)及microRNAs(miRNAs)在调控基因的表达方面扮演了重要的角色。TFs和miRNAs之间存在广泛的相互作用和合作调控,共同组成复杂的调控网络,对于了解细胞的生理过程、生物学功能、疾病的发生机制等都起到了重要作用。目前面临的首要难题是骨肉瘤往往不能做到早期诊断,诊断不及时会耽误治疗时机,严重影响患者预后[2-3]。因此,建立新的、有效的骨肉瘤防治措施势在必行,还需寻找并发现新的功能基因靶向治疗骨肉瘤,根据治疗效果建立分子水平预后指标,开发安全的不同于传统治疗骨肉瘤的放化疗药物,是当前科研及临床研究中的热门话题[4-5]。本研究将利用高通量基因芯片技术分析骨肉瘤中差异表达的基因和miRNAs,结合生物信息学软件预测与调控骨肉瘤相关的TFs、miRNAs及其靶基因,分析调控网络中的关键基因及关键miRNAs的功能,构建骨肉瘤发生发展的“TFs-miRNAs”共调控网络。
1 材料与方法
1.1 miRNA数据来源
收集美国国家生物技术信息中心(National Center of Biotechnology Information, NCBI)维护的GEO数据库中的两组数据库(GPL8227、GPL19631)中所有骨肉瘤miRNA数据,收集数据时间截至2016年12月31日。
1.2 数据库资源
用基因本体论数据库(gene ontology, GO)对所分析得到的差异表达基因进行功能注释;使用京都基因与基因组百科全书(kyoto encyclopedia of genes and genomes, KEGG)数据库对差异表达基因进行代谢通路富集分析;使用转录作用元件数据库(transcriptional regulatory element database, TRED)对差异表达基因进行转录因子筛选。
1.3 方法
1.3.1 差异表达基因筛选及注释
为探究骨肉瘤细胞发生发展的分子机制,用R语言下载GEO数据库中GSE28425、GSE65071数据集的原始数据。使用MAS 5.0算法对数据集中的原始数据进行标准化预处理。使用Limma程序包中所提供的统计分析函数,计算与健康者细胞系相比,骨肉瘤患者中表达水平发生变化的基因。选取差异表达倍数≥2.0(Fold Change≥2.0)为筛选阈值,筛选获得差异表达的miRNA。通过差异表达分析获得两组平台共有的骨肉瘤细胞系表达水平发生显著性改变的miRNA,利用DIANA TOOLS数据库中收录的人类基因信息,找到具有显著差异的miRNA靶基因。利用R语言,将筛选得到的差异表达基因与GEO数据库提供的GPL平台注释信息进行匹配,对差异表达基因进行信息注释。
1.3.2 差异表达基因KEGG代谢通路富集分析
为进一步探究差异表达基因参与生物代谢的代谢通路,对筛选得到的差异表达基因进行KEGG代谢通路富集分析。提取差异表达基因GPL平台注释信息中的“Entrez_Gene_ID”信息,应用R语言KEGG程序包与KEGG数据库信息,对每一个差异表达基因向已知的代谢通路进行富集映射,探究差异表达基因集中映射的细胞代谢通路,初步推测骨肉瘤所影响的主要代谢通路,并筛选出与肿瘤通路关系密切的基因,进行GO功能注释分析。
1.3.3 差异表达基因GO功能注释分析
为探究差异表达且与肿瘤通路关系密切的基因所参与的生物功能,对筛选得到的与肿瘤通路关系密切的差异表达基因进行GO功能注释分析。提取差异表达基因GPL平台注释信息中的“Entrez_Gene_ID”信息,使用R语言GO程序包与GO数据库信息,对每一个差异表达基因进行功能注释,探究骨肉瘤组织与正常组织差别的基因功能,初步推测骨肉瘤作用的分子机制。
1.3.4 分子共调控网络构建
为进一步挖掘骨肉瘤的分子调控模式,探究差异表达基因之间的相互调控作用关系,提取TRED数据库中所收录的所有人类转录因子数据。通过Pearson相关性分析,提取基因间分子共调控作用关系。使用Cytoscape version 3.4.0软件对得到的分子共调控作用关系进行可视化展示,构建出最终的分子共调控网络。
2 结果
2.1 差异表达基因的筛选
本研究分别从GPL8227、GPL19631两组数据库中筛选出差异表达miRNA 232个(上调129个、下调103个)和265个(上调205个、下调60个)。共筛选得到两组均包含的差异表达miRNA52个,其中31个miRNA上调表达,21个miRNA下调表达见表 1。
表 1 差异表达的miRNAs信息Table 1 Information of differentially-expressed miRNAs
2.2 差异表达基因KEGG代谢通路富集分析
将筛选出的52个差异表达miRNA结合DIANA TOOLS数据库中收录的人类基因信息进行分析。其中KEGG代谢通路富集分析结果见图 1,差异表达基因主要参与肿瘤相关的诸多代谢通路。差异表达的52个miRNA的整体调控模式及每个miRNA所调控的代谢通路情况见图 2。肿瘤代谢通路的分子调控关系网络见图 3。
2.3 差异表达基因GO功能注释分析
将上述筛选出与肿瘤通路关系最紧密的5个miRNA及其靶基因进行GO功能注释分析。注释分析结果显示这些基因主要参与维生素E的代谢路径(response to vitamin E)、RNA聚合酶Ⅱ启动子的转录调控反应(regulation of transcription from RNA polymerase Ⅱ promoter in response etc)、调控神经元的成熟(regulation of neuron maturation)、受体激动剂活性(receptor agonist activity)、正调控血管内皮生长因子受体活性(positive regulation of vascular endothelial growth factor receptor activity)、通过MAPK级联非经典Wnt信号途径(non-canonical wnt signaling pathway via MAPK cascade)、间充质上皮细胞信号转导(mesenchymal-epithelial cell signaling)、Ⅳ型胶原(collagen type Ⅳ)、细胞对生长激素刺激的反应(cellular response to growth hormone stimulus)、蛋白激酶活性的激活(activation of protein kinase A activity)等生物功能,见图 4。
2.4 分子共调控网络构建
最后基于与肿瘤通路密切相关的差异表达基因及TRED数据库中所收录的人类转录因子信息,对差异表达基因进行分子偶联,构建了分子共调控网络,见图 5。
3 讨论
目前miRNA被广泛认为是血液学和肿瘤组织的生物标志物。miRNA有可能通过扭曲、突变、成纤维细胞生长因子(FGF)和骨形态发生蛋白(BMP)信号参与骨的形成。研究发现miRNA与多种骨科疾病有关系,比如有研究认为miRNA-140与骨性关节炎有关,miRNA-503、miRNA-3960与骨质疏松有关,miRNA-34、miRNA-146等与类风湿关节炎有关[6]。研究表明众多的miRNA在骨肉瘤发病的机制中异常表达,被miRNA决定的许多基因被上调或下调。比如Karbasy等[7]通过研究发现miR-125b和miR-300的下调与骨肉瘤的进展相关且两者都起到抑癌基因的作用。Goudarzi等[8]通过研究发现miR-185上调miR-218下调与软骨肉瘤的进展相关联,并且两者均可以作为软骨肉瘤的抑癌基因。Bahador等[9]通过研究发现在青少年、儿童以及青年人骨肉瘤患者中,如果miR-29b和miR-422a的表达下调往往表明患者的预后较差。Taheriazam等[10]通过研究发现下调microRNA-26a和微小RNA-27A的上调有助于判断人类骨肉瘤的攻击性进展。高表达的miR-130b水平和miR-218的低表达与差的临床病理特征有关。此外,有研究表明miR-130b可对预测骨肉瘤的进展起关键作用[10-11]。另有研究表明miR-145、miR-128、miR-34a在骨肉瘤中的表达均发生了改变。miR-335、miR-128、miR-340、miR-214等均与骨肉瘤的侵袭性有重要关系,表达增高后预示骨肉瘤的恶性程度较高,可以较早发生转移,患者的生存期缩短[12]。并且近期有研究表明血浆中miR-34b表达下降可能与骨肉瘤已经发生转移有密切的联系[13],如果能明确这种作用关系会对骨肉瘤的早期诊断起到非凡的作用。就目前研究现状来看骨肉瘤发生发展的分子作用机制尚不十分明确,本研究利用高通量基因芯片技术,通过生物信息学手段,系统性预测构建了一张与肿瘤通路关系密切的TF、miRNA及其靶基因共调控网络蓝图。该分子共调控网络从整体的角度鸟瞰与肿瘤通路关系密切的miRNA及其靶基因的相互作用关系,展示了差异表达基因主要参与肿瘤相关的诸多代谢通路及与肿瘤通路有关的基因主要参与的生物功能。为骨肉瘤诊断标志物簇的筛选提供可靠的选择方向;为临床诊断及预后分析分子靶点的筛选提供实用工具,同时也为其他癌症的同类研究提供新思路。
作者贡献黄 平:实施研究,数据分析,文章撰写
窦长武:提出研究思路,设计研究方案
鞠海涛、王宏伟:指导实验,获取研究经费
肖 瑞:修改文章内容
牛丽丽:指导实验,采集数据 -
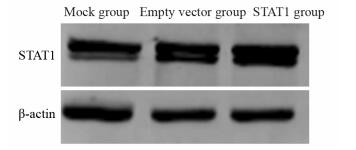
表 1 转染pcDNA3.1-STAT1后胶质瘤U251细胞STAT1蛋白的表达
Table 1 Expression of STAT1 protein in glioma U251 cells after transfection with pcDNA3.1-STAT1

表 2 各组各时间点脑胶质瘤U251细胞增殖活性测定(x±s)
Table 2 Proliferation activity of glioma U251 cells at different time points in each group (x±s)

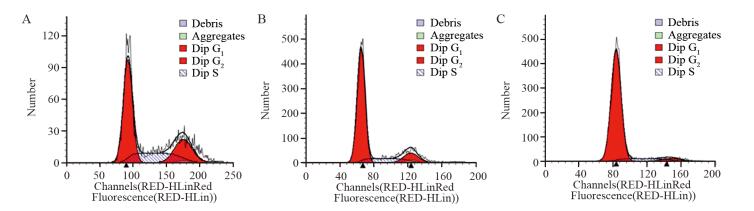
表 3 转染48h后STAT1对脑胶质瘤U251细胞周期的影响
Table 3 Effect of STAT1 on cell cycle of glioma U251 cells 48h after transfection

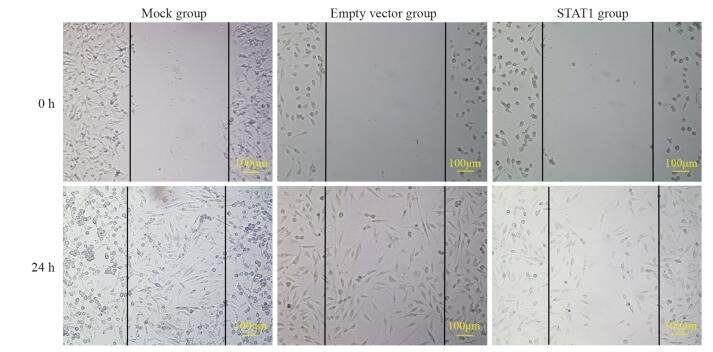
表 4 细胞划痕实验检测转染pcDNA3.1-STAT1 24h后对胶质瘤U251细胞迁移能力的影响
Table 4 Migration ability of U251 cells after transfection with pcDNA3.1-STAT1 for 24h detected by wound healing assay

表 5 P53、P21、bcl-2、Caspase-8在转染pcDNA3.1-STAT1脑胶质瘤U251细胞中的表达(x±s)
Table 5 Expression of P53, P21, bcl-2 and Caspase-8 in U251 cells after transfection with pcDNA3.1-STAT1 (x±s)

-
[1] Ostrom QT, Gittleman H, Truitt G, et al. CBTRUS statistical report: primary brain and other central nervous system tumors diagnosed in the united states in 2011-2015[J]. Neuro Oncol, 2018, 20(suppl_4): iv1-iv86. doi: 10.1093/neuonc/noy131
[2] Stark GR, Darnell JE Jr. The JAK-STAT pathway at twenty[J]. Immunity, 2012, 36(4): 503-14. doi: 10.1016/j.immuni.2012.03.013
[3] Monnier A, Boniface R, Bouvet R, et al. The expression of EMX2 lead to cell cycle arrest in glioblastoma cell line[J]. BMC Cancer, 2018, 18(1): 1213. doi: 10.1186/s12885-018-5094-y
[4] Munoz JL, Rodriguez-Cruz V, Ramkissoon SH, et al. Temozolomide resistance in glioblastoma occurs by miRNA-9-targeted PTCH1, independent of sonic hedgehog level[J]. Oncotarget, 2015, 6(2): 1190-201.
[5] Waghmare I, Roebke A, Minata M, et al. Intercellular cooperation and competition in brain cancers: lessons from Drosophila and human studies[J]. Stem Cells Transl Med, 2014, 3(11): 1262-8. doi: 10.5966/sctm.2014-0086
[6] Castro MG, Candolfi M, Kroeger K, et al. Gene therapy and targeted toxins for glioma[J]. Curr Gene Ther, 2011, 11(3): 155-80. doi: 10.2174/156652311795684722
[7] 毛颖, 花玮.精准神经外科:从宏观到微观[J].中华医学杂志, 2015, 95(31): 2510-1. doi: 10.3760/cma.j.issn.0376-2491.2015.31.006 Mao Y, Hua W. Application of precision medicine for neurosurgery[J]. Zhonghua Yi Xue Za Zhi, 2015, 95(31): 2510-1. doi: 10.3760/cma.j.issn.0376-2491.2015.31.006
[8] Brivanlou AH, Darnell JE Jr. Signal transduction and the control of gene expression[J]. Science, 2002, 295(5556): 813-8. doi: 10.1126/science.1066355
[9] Noack K, Mahendrarajah N, Hennig D, et al. Analysis of the interplay between all-trans retinoic acid and histone deacetylase inhibitors in leukemic cells[J]. Arch Toxicol, 2017, 91(5): 2191-208. doi: 10.1007/s00204-016-1878-5
[10] Hou Y, Li X, Li Q, et al. STAT1 facilitates oestrogen receptor α transcription and stimulates breast cancer cell proliferation[J]. J Cell Mol Med, 2018, 22(12): 6077-86. doi: 10.1111/jcmm.2018.22.issue-12
[11] Narkwa PW, Blackbourn DJ, Mutocheluh M. Aflatoxin B1 inhibits the type 1 interferon response pathway via STAT1 suggesting another mechanism of hepatocellular carcinoma[J]. Infect Agent Cancer, 2017, 12: 17. doi: 10.1186/s13027-017-0127-8
[12] Meissl K, Macho-Maschler S, Müller M, et al. The good and the bad faces of STAT1 in solid tumours[J]. Cytokine, 2017, 89: 12-20. doi: 10.1016/j.cyto.2015.11.011
[13] Zhang Y, Jin G, Zhang J, et al. Overexpression of STAT1 suppresses angiogenesis under hypoxia by regulating VEGF-A in human glioma cells[J]. Biomed Pharmacother, 2018, 104: 566-75. doi: 10.1016/j.biopha.2018.05.079
[14] Ju H, Li X, Li H, et al. Mediation of multiple pathways regulating cell proliferation, migration, and apoptosis in the human malignant glioma cell line U87MG via unphosphorylated STAT1[J]. J Neurosurg, 2013, 118(6): 1239-47. doi: 10.3171/2013.3.JNS122051
[15] Yang W, Wang H, Dou C, et al. A study on the correlation between STAT-1 and mutant p53 expression in glioma[J]. Mol Med Rep, 2018, 17(6): 7807-12.
[16] Hainaut P, Wiman KG. 30 years and a long way into p53 research[J]. Lancet Oncol, 2009, 10(9): 913-9. doi: 10.1016/S1470-2045(09)70198-6
[17] Karimian A, Ahmadi Y, Yousefi B. Multiple functions of p21 in cell cycle, apoptosis and transcriptional regulation after DNA damage[J]. DNA Repair (Amst), 2016, 42: 63-71. doi: 10.1016/j.dnarep.2016.04.008
[18] Chen G, Wang H, Xie S, et al. STAT1 negatively regulates hepatocellular carcinoma cell proliferation[J]. Oncol Rep, 2013, 29(6): 2303-10. doi: 10.3892/or.2013.2398
[19] Chen J, Wang H, Wang J, et al. STAT1 inhibits human hepatocellular carcinoma cell growth through induction of p53 and Fbxw7[J]. Cancer Cell Int, 2015, 15: 111. doi: 10.1186/s12935-015-0253-6
[20] Atkins KM, Thomas LL, Barroso-González J, et al. The multifunctional sorting protein PACS-2 regulates SIRT1-mediated deacetylation of p53 to modulate p21-dependent cell- cycle arrest[J]. Cell Rep, 2014, 8(5): 1545-57. doi: 10.1016/j.celrep.2014.07.049
[21] Dimco G, Knight RA, Latchman DS, et al. STAT1 interacts directly with cyclin D1/Cdk4 and mediates cell cycle arrest[J]. Cell Cycle, 2010, 9(23): 4638-49. doi: 10.4161/cc.9.23.13955
[22] Yamasaki L. Role of the RB tumor suppressor in cancer[J]. Cancer Treat Res, 2003, 115: 209-39. http://d.old.wanfangdata.com.cn/OAPaper/oai_pubmedcentral.nih.gov_2716981
[23] Shakeel E, Sharma N, Akhtar S, et al. Decoding the antineoplastic efficacy of Aplysin targeting Bcl-2: A de novo perspective[J]. Comput Biol Chem, 2018, 77: 390-401. doi: 10.1016/j.compbiolchem.2018.09.003
[24] Valentin R, Grabow S, Davids MS, et al. The rise of apoptosis: targeting apoptosis in hematologic malignancies[J]. Blood, 2018, 132(12): 1248-64. doi: 10.1182/blood-2018-02-791350
[25] Xue M, Ge Y, Yu C, et al. Apoptosis is induced by docosahexaenoic acid in breast cancer cells via death receptor and mitochondria-mediated pathways[J]. Mol Med Rep, 2017, 16(1): 978-82. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=728f6d74a10f1aca2d95337a76c4009d
[26] Werner AB, de Vries E, Borst J, et al. Bcl-2 family member Bfl-1/A1 sequesters truncated bid to inhibit is collaboration with pro-apoptotic Bak or Bax[J]. J Biol Chem, 2002, 277(25): 22781-8. doi: 10.1074/jbc.M201469200
-
期刊类型引用(1)
1. 冯晓慧,朱正秋. NLR对晚期食管鳞癌一线免疫治疗疗效的预测价值. 医学研究杂志. 2023(07): 157-160+123 .  百度学术
百度学术
其他类型引用(2)



 下载:
下载: