-
摘要:
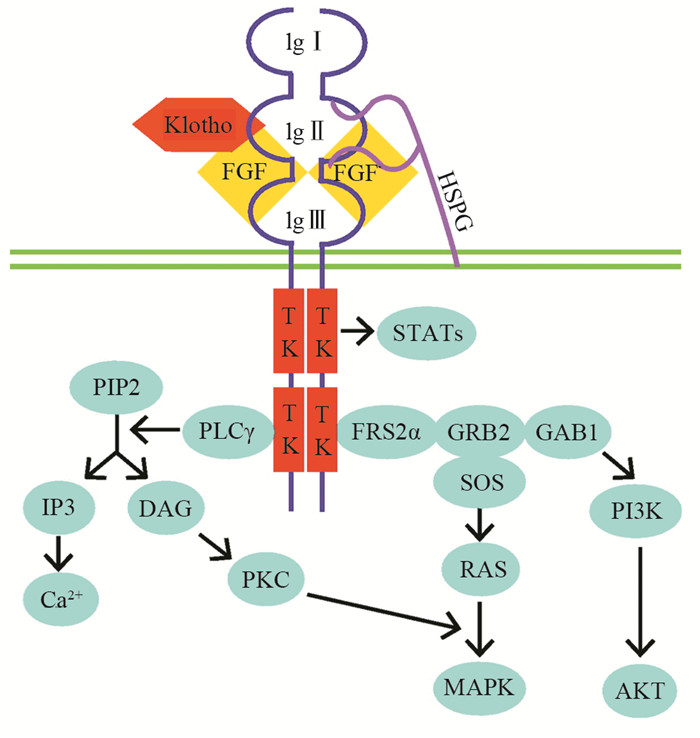
成纤维细胞生长因子受体4(FGFR4)通过启动STAT3、MAPK和PI3K/AKT等信号级联,调节细胞的增殖、分化和转移。其基因突变、过表达或其配体分子过表达等异常信号转导在某些肿瘤的发生发展中发挥着重要的作用,表明FGFR4是此类肿瘤潜在的治疗靶标。靶向FGFR4的抗肿瘤药物或方法主要包括小分子抑制剂、单克隆抗体、配体捕获蛋白、短链RNA寡核苷酸适配体(shRNA)。本文回顾FGFR4异常的肿瘤及靶向FGFR4抗肿瘤药物的研究进展。
-
关键词:
- 成纤维细胞生长因子受体4 /
- 肿瘤 /
- 信号通路 /
- 小分子抑制剂 /
- 单克隆抗体
Abstract:Activated fibroblast growth factor receptor 4 (FGFR4) initiates STAT3, MAPK and PI3K/AKT signaling cascades, regulates the proliferation, differentiation and migration of cells. The FGFR4 signaling aberrations, such as mutation, overexpression or ligand overexpression, play crucial roles in the genesis and development of various tumor cells. It indicates that FGFR4 is a potential therapy target. Blocking FGFR4 signaling pathway is an effective method for treating tumors with FGFR4 signaling aberrations, which containing small molecule kinase inhibitor, monoclonal antibody, ligand capture protein and short RNA oligonucleotide adapter (shRNA). In this paper, we reviewed the abnormal signaling of FGFR4 in tumor and the research progress of anti-tumor drug.
-
Key words:
- FGFR4 /
- Tumor /
- Signaling pathway /
- Small-molecule inhibitor /
- Monoclonal antibody
-
0 引言
白血病发病率相对较小[1],但生存率较低(19.6%)[2],因此,严重影响儿童及老年人的身体健康,是造成居民巨大疾病负担的癌症之一[3-4]。昆山市位居上海与苏州之间,特殊的区位优势使得近20年经济社会快速发展,在昆山市肿瘤粗死亡率明显上升的背景下[5],本研究利用1993—2014年昆山市死因监测的白血病死亡数据,以探究其死亡率的时间趋势。
1 资料与方法
1.1 研究对象来源
江苏省昆山市于1981年全面开展全人群死因监测工作[5]。昆山市所有社区卫生服务机构及医院开展死因常规监测,同时疾控中心通过定期与公安、殡葬、妇幼保健及福利院等多部门合作,多途径收集死亡名单并开展死亡原因调查;市镇两级从业人员通过定期举办培训班、认真规范填写死亡证、逐条数据审核、现场督导检查及定期开展漏报调查等方式,来保证全市死因监测工作的质量。此外,也与苏州市范围内的其他县(市)进行数轮的数据质量互审,重点对数据的完整性、原始数据的逻辑性、统计分类及ICD-10编码以及是否重卡等进行检查、修正。昆山市所有死亡病例开具《居民死亡医学证明(推断)书》其登记报告项目包括:(1)病例人口学特征(姓名、性别、出生日期、民族、婚姻、文化程度、职业等)。(2)死亡信息:死亡原因(直接死因、间接死因、根本死因以及其他重要医学情况)、死亡日期、死亡地点等。(3)诊断信息:疾病最高诊断单位、疾病最高诊断依据等内容。(4)调查记录。年初与年末人口数来源于昆山市公安局,以计算年均观察人年数,1981—2013年年均观察人年数(年均人口数)详参文献[5]。
按照《国际疾病分类》(ICD-10)对所有恶性肿瘤疾病进行编码,白血病ICD-10编码为C91-95。根据《中国肿瘤登记工作指导手册》,并参照国际癌症研究中心(IARC)/国际癌症登记协会(IACR)对登记材料的有关要求,对肿瘤登记的完整性和可靠性进行了评估。
1.2 数据分析
采用SAS9.3统计软件进行数据分析,计算年份、性别粗死亡率与年龄标化死亡率,以及绘制时间趋势图和年龄别死亡率序列图。按照第五次全国人口普查(2000年)人口结构为标准计算年龄标化死亡率。应用年度变化百分比(annual percentage change, APC)及其95%可信区间(confidence intervals, CI)分析粗死亡率与年龄标化死亡率等时间趋势,以APC其95%CI是否包含0为统计学检验标准,同时给出回归系数检验的P值[6]。
2 结果
2.1 江苏省昆山市1993—2014年白血病死亡趋势分析
江苏省昆山市1993—2014年期间白血病死亡总例数为570例(男312例,女258例),占全肿瘤比例为2.19%;总的来看昆山市1993—2014年白血病死亡数明显上升(APC=3.0, 95%CI: 1.6~4.4, P=0.0007)。
江苏省昆山市白血病粗死亡率由1993年的4.01/10万上升到2014年的4.99/10万,上升趋势没有统计学意义(APC=1.5, 95%CI: 0.0~3.0, P=0.0604)。在男性人群中白血病粗死亡率由1993年的4.53/10万上升到2014年的5.02/10万,上升趋势无明显统计学意义(APC=0.8, 95%CI: -0.6~2.2, P=0.2756);女性人群中白血病粗死亡率由1993年的3.49/10万上升到2014年的4.96/10万,上升趋势无统计学意义(APC=2.7, 95%CI: 0.0~5.4, P=0.0622)。1993—2014年白血病中标死亡率在男女合计人群中无明显变化趋势(APC=1.5, 95%CI: 0.0~3.0, P=0.0604);男性(APC=-0.7, 95%CI: -2.4~1.0, P=0.4087)和女性(APC=0.4, 95%CI: -2.3~3.1, P=0.7612)人群中白血病中标死亡率没有明显变化趋势,见图 1、表 1。
1993—2014年白血病死亡率其0~74岁累积死亡率由1993年的0.33%上升到2014年的0.38%(APC=0.7, 95%CI: -0.9~2.3, P=0.4168),没有发现白血病死亡的风险在0~74岁年龄组随着时间有明显变化,见表 1。
表 1 江苏省昆山市1993—2014年白血病死亡率分析Table 1 Mortality of leukemia in Kunshan City, Jiangsu Province, 1993-2014
2.2 江苏省昆山市1993—2014年白血病年龄别死亡率分析
1993—2004年,白血病年龄别死亡率在60之前处于低水平,60岁以后缓慢上升,至65~69岁达到高峰,70岁以后白血病死亡率明显下降。2005—2014年,白血病年龄别死亡率在60之前处于低水平,60岁以后开始明显抬升,至70~74岁达到高峰,75岁以后白血病死亡率略有下降。与1993—2004年相比,2005—2014年白血病年龄别死亡率明显偏高,特别是60岁以上年龄段,见图 2、表 2。
表 2 江苏省昆山市白血病年龄别死亡率分析Table 2 Age-specific mortality of leukemia by gender in Kunshan City, Jiangsu Province
3 讨论
在江苏省昆山市肿瘤中标死亡率总体呈现下降趋势的情况下[5],人口老龄化与其他危险因素一起促进了肿瘤死亡的变化。在昆山市肿瘤死亡率明显上升的肺癌中这种促进因素最为明显[7]。虽然昆山市白血病占全肿瘤死亡(2.19%)的比例较低;但是由于发病年龄较早、生存率较低及预后差[2],造成的疾病负担较大。
昆山市白血病死亡率位居肿瘤死亡顺位第9位[8-9]。同期与全国白血病死亡率相比,昆山地区死亡率明显低于全国2009年水平(世标率,2.66/10万 vs. 3.35/10万)[10],也低于全国2012年水平(2.48/10万 vs. 3.13/10万)[11]。就死亡率趋势来看,昆山市1993—2014年白血病中标死亡率趋势则没有明显的变化(APC=1.5, 95%CI: 0.0~3.0, P=0.0604)。浙江省2000—2009年白血病死亡率明显上升(APC=5.09, 95%CI: 1.13~9.21)[12],此外还有山东省(1970—2005年)[13]。除了单独看白血病死亡率,白血病发病率的高低不容忽视。与昆山市相邻的浙江省2000—2009年白血病的发病率明显上升(APC=3.21, 95%CI: 0.20~6.30)[12],此外上海[14]与南京地区[4]白血病发病率也明显上升。
从白血病年龄别死亡率来看,本研究显示白血病年龄别死亡率呈现明显的两个高峰,即20岁以下年龄组与65岁以上年龄组,与上海和浙江等地区的研究结果基本一致[4, 12, 14];也与全国肿瘤登记的结果一致[15]。年龄别死亡率的差异提示白血病的发病可能是暴露因素的差异所致。白血病的发生是基因与环境共同作用的结果。经济社会状态也是影响白血病发生的因素[16]。环境因素中饮食模式是影响白血病发生的因素之一[17-18];父母早期的不良生活方式暴露是影响儿童白血病的因素,如烟草、酒精等[19-20]。
虽然江苏省昆山市1993—2014年白血病死亡率趋势变化不明显;但是随着户籍人口逐年增加,因白血病而死亡的例数明显上升,疾病负担加大。在继续强化监测工作以观察其时间趋势的同时,也要考虑进一步加强监测工作质量控制。江苏省昆山市于1981年全面开展死因监测[5];在2013年加入国家疾病监测点,在加入监测点之前于2011—2012年开展了死亡漏报调查,结果显示漏报率为0.34%,提示既往的死因监测处于可接受区间[21]。
-
表 1 靶向FGFR4的抗肿瘤药物
Table 1 FGFR4 targeted anti-tumor drug

-
[1] Dienstmann R, Rodon J, Prat A, et al. Genomic aberrations in the FGFR pathway: opportunities for targeted therapies in solid tumors[J]. Ann Oncol, 2013, 25(3): 552-63. https://www.researchgate.net/publication/258830759_Genomic_aberrations_in_the_FGFR_pathway_Opportunities_for_targeted_therapies_in_solid_tumors
[2] 王明, 孙震宇, 黄礼年. FGF/FGFR信号通路在肺鳞癌靶向治疗中的研究进展[J].肿瘤防治研究, 2016, 43(7): 638-44. http://www.zlfzyj.com/CN/abstract/abstract8804.shtml Wang M, Sun ZY, Huang LN. Advances of FGF/FGFR signaling pathway in targeted therapy for squamous cell lung cancer[J]. Zhong Liu Fang Zhi Yan Jiu, 2016, 43(7): 638-44. http://www.zlfzyj.com/CN/abstract/abstract8804.shtml
[3] Tenhagen M, van Diest PJ, Ivanova IA, et al. Fibroblast growth factor receptors in breast cancer: expression, downstream effects, and possible drug targets[J]. Endocr Relat Cancer, 2012, 19(4):R115-29. doi: 10.1530/ERC-12-0060
[4] Desai A, Adjei AA. FGFR Signaling as a Target for Lung Cancer Therapy[J]. J Thorac Oncol, 2016, 11(1): 9-20. doi: 10.1016/j.jtho.2015.08.003
[5] Lu C, Huguley S, Cui C, et al. Effects of FGFR Signaling on Cell Proliferation and Differentiation of Apert Dental Cells[J]. Cells Tissues Organs, 2016, 201(1): 26-37. https://www.researchgate.net/publication/284879913_Effects_of_FGFR_Signaling_on_Cell_Proliferation_and_Differentiation_of_Apert_Dental_Cells?_sg=4GT73fkTj8l4kEMNOcNVuxBcObYYBP17yCYQXLsNy22OU93jRQs7c4pxhBS_QeGRLLgSL7QISFkvobyqcjDIOQ
[6] Crose LE, Etheridge KT, Chen C, et al. FGFR4 blockade exerts distinct antitumorigenic effects in human embryonal versus alveolar rhabdomyosarcoma[J]. Clin Cancer Res, 2012, 18(14): 3780-90. doi: 10.1158/1078-0432.CCR-10-3063
[7] André F, Cortés J. Rationale for targeting fibroblast growth factor receptor signaling in breast cancer[J]. Breast Cancer Res Treat, 2015, 150(1): 1-8. doi: 10.1007/s10549-015-3301-y
[8] Cho SH, Shin MH, Kweon SS, et al. FGFR4 Arg388 polymorphism is a poor prognostic factor for resected stage Ⅲ colon cancer[J]. Cancer Res, 2015, 75(15 Supplement): 3407. doi: 10.1158/1538-7445.AM2015-3407
[9] Shimada Y, Okumura T, Takei Y, et al. Role of fibroblast growth factor receptors in esophageal squamous cell carcinoma[J]. Esophagus, 2016, 13(1): 30-41. doi: 10.1007/s10388-015-0486-4
[10] Zhou W, Du X, Song F, et al. Prognostic roles for fibroblast growth factor receptor family members in malignant peripheral nerve sheath tumor[J]. Oncotarget, 2016, 7(16): 22234-44. https://www.researchgate.net/publication/299073842_Prognostic_roles_for_fibroblast_growth_factor_receptor_family_members_in_malignant_peripheral_nerve_sheath_tumor
[11] Hagel M, Miduturu C, Sheets M, et al. First selective small molecule inhibitor of FGFR4 for the treatment of hepatocellular carcinomas with an activated FGFR4 signaling pathway[J]. Cancer Discov, 2015, 5(4): 424-37. doi: 10.1158/2159-8290.CD-14-1029
[12] Ishiwata T, Yoshimura H, Matsuda Y, et al. Fibroblast growth factor receptor-4 (FGFR-4) as a novel therapeutic target for pancreatic cancer[J]. Cancer Res, 2016, 76(14 Supplement): 4577. doi: 10.1158/1538-7445.AM2016-4577
[13] Sequist LV, Cassier P, Varga A, et al. Abstract CT326: Phase I study of BGJ398, a selective pan-FGFR inhibitor in genetically preselected advanced solid tumors[J]. Cancer Res, 2014, 74(19 Supplement): CT326. doi: 10.1158/1538-7445.AM2014-CT326
[14] Lesca E, Lammens A, Huber R, et al. Structural Analysis of the Human Fibroblast Growth Factor Receptor 4 Kinase[J]. J Mol Biol, 2014, 426(22): 3744-56. doi: 10.1016/j.jmb.2014.09.004
[15] Li SQ, Cheuk AT, Shern JF, et al. Targeting wild-type and mutationally activated FGFR4 in rhabdomyosarcoma with the inhibitor ponatinib (AP24534)[J]. PLoS One, 2013, 8(10): e76551. doi: 10.1371/journal.pone.0076551
[16] Nakanishi Y, Akiyama N, Tsukaguchi T, et al. The fibroblast growth factor receptor genetic status as a potential predictor of the sensitivity to CH5183284/Debio 1347, a novel selective FGFR inhibitor[J]. Mol Cancer Ther, 2014, 13(11): 2547-58. doi: 10.1158/1535-7163.MCT-14-0248
[17] Ye YW, Hu S, Shi YQ, et al. Combination of the FGFR4 inhibitor PD173074 and 5-fluorouracil reduces proliferation and promotes apoptosis in gastric cancer[J]. Oncol Rep, 2013, 30(6): 2777-84. http://or.nsfc.gov.cn/handle/00001903-5/376228
[18] Ader I, Delmas C, Skuli N, et al. Preclinical evidence that SSR128129E-A novel small-molecule multi-fibroblast growth factor receptor blocker-Radiosensitises human glioblastoma[J]. Eur J Cancer, 2014, 50(13): 2351-9. doi: 10.1016/j.ejca.2014.05.012
[19] Tie J, Bang YJ, Park YS, et al. Abstract CT215: A phase I trial of LY2874455, a fibroblast growth factor receptor inhibitor, in patients with advanced cance[J]. Cancer Res, 2014, 74(19 Supplement): CT215. doi: 10.1158/1538-7445.AM2014-CT215
[20] Tabernero J, Bahleda R, Dienstmann R, et al. PhaseⅠDose-Escalation Study of JNJ-42756493, an Oral Pan-Fibroblast Growth Factor Receptor Inhibitor, in Patients With Advanced Solid Tumors[J]. J Clin Oncol, 2015, 33(30): 3401-8. doi: 10.1200/JCO.2014.60.7341
[21] Repana D, Ross P. Targeting FGF19/FGFR4 pathway: A novel therapeutic strategy for hepatocellular carcinoma[J]. Diseases, 2015, 3(4): 294-305. doi: 10.3390/diseases3040294
[22] Bange J, Niewoehner J, Dem Siepen PA, et al. FGFR4 antibodies: U.S. Patent 8, 394, 927[P]. 2013-3-12.
[23] Dennis M, Desnoyers L, French D. Anti-FGFR4 antibodies and methods of use: U.S. Patent 9, 266, 955[P]. 2016-2-23.
[24] Bartz R, Fukuchi K, Lange T, et al. U3-1784, a human anti-FGFR4 antibody for the treatment of cancer[J]. Cancer Res, 2016, 76(14 Supplement): Abstract 3852. doi: 10.1158/1538-7445.AM2016-3852
[25] Pai R, French D, Ma N, et al. Antibody-mediated inhibition of fibroblast growth factor 19 results in increased bile acids synthesis and ileal malabsorption of bile acids in cynomolgus monkeys[J]. Toxicol Sci, 2012, 126(2): 446-56. doi: 10.1093/toxsci/kfs011
[26] Tolcher AW, Papadopoulos KP, Patnaik A, et al. A Phase Ⅰ, first in human study of FP-1039 (GSK3052230), a novel FGF ligand trap, in patients with advanced solid tumors[J]. Ann Oncol, 2016, 27(3): 526-32. doi: 10.1093/annonc/mdv591
[27] Zaid TM, Yeung TL, Thompson MS, et al. Identification of FGFR4 as a potential therapeutic target for advanced-stage, high-grade serous ovarian cancer[J]. Clin Cancer Res, 2013, 19(4): 809-20. doi: 10.1158/1078-0432.CCR-12-2736
[28] Heinzle C, Gsur A, Hunjadi M, et al. Differential effects of polymorphic alleles of FGF receptor 4 on colon cancer growth and metastasis[J]. Cancer Res, 2012, 72(22): 5767-77. doi: 10.1158/0008-5472.CAN-11-3654
[29] Ye Y, Jiang D, Li J, et al. Silencing of FGFR4 could influence the biological features of gastric cancer cells and its therapeutic value in gastric cancer[J]. Tumour Biol, 2016, 37(3): 3185-95. doi: 10.1007/s13277-015-4100-0
[30] 宋艳宁, 张赫然, 尹东东, 等.小分子酪氨酸激酶抑制剂在癌症靶向治疗的研究进展[J].中国药学杂志, 2016, 51(3): 165-71. http://www.cnki.com.cn/Article/CJFDTOTAL-ZGYX201603001.htm Song YN, Zhang HR, Yin DD, et al. Advances in research of small molecule tyrosine kinase inhibitors for targeted cancer therapy[J]. Zhongguo Yao Xue Za Zhi, 2016, 51(3): 165-71. http://www.cnki.com.cn/Article/CJFDTOTAL-ZGYX201603001.htm
[31] Fan J, Dai Y, Shao J, et al. Design, synthesis and biological evaluation of pyrazolylaminoquinazoline derivatives as highly potent pan-fibroblast growth factor receptor inhibitors[J]. Bioorg Med Chem Lett, 2016, 26(11): 2594-9. doi: 10.1016/j.bmcl.2016.04.028
[32] Zhao G, Li WY, Chen D, et al. A novel, selective inhibitor of fibroblast growth factor receptors that shows a potent broad spectrum of antitumor activity in several tumor xenograft models[J]. Mol Cancer Ther, 2011, 10(11): 2200-10. doi: 10.1158/1535-7163.MCT-11-0306
[33] Andre F, Ranson M, Dean E, et al. Abstract LB-145: Results of a phase I study of AZD4547, an inhibitor of fibroblast growth factor receptor (FGFR), in patients with advanced solid tumors[J]. Cancer Res, 2013, 73(8 Supplement): LB-145. doi: 10.1158/1538-7445.AM2013-LB-145
[34] French DM, Lin BC, Wang M, et al. Targeting FGFR4 inhibits hepatocellular carcinoma in preclinical mouse models[J]. PLoS One, 2012, 7(5): e36713. doi: 10.1371/journal.pone.0036713




 下载:
下载: